
De afgelopen decennia van mijn carrière heb ik talloze uren besteed aan het beschermen van Amerikanen door onderzoek te doen naar de veiligheid van drugs. Mijn opleiding en carrière hebben mij langs een zestal universiteiten, Big Pharma en bij de FDA geleid onder drie presidentiële regeringen. Bij de geneesmiddelenveiligheid wordt rekening gehouden met de vraag waarom het ene individu een farmaceutisch product kan gebruiken en geen bijwerkingen ondervindt, terwijl een ander individu hetzelfde product kan gebruiken, maar bijwerkingen kan hebben die kunnen leiden tot blijvende invaliditeit of overlijden. Bij het bestuderen van de veiligheid van geneesmiddelen wordt standaard ook rekening gehouden met niet-klinische aspecten van de productie en de kwaliteit van geneesmiddelen.
Omdat de kwaliteit van medicijnen een essentiële factor is bij het beoordelen van de veiligheid van medicijnen, heeft mijn tocht om de Amerikanen te beschermen geleid tot het conceptualiseren en oprichten van ‘s werelds eerste ‘analytische apotheek” met de opdracht om farmaceutische producten uit plaatsen als India en China wetenschappelijk te verifiëren voordat ze aan patiënten worden verstrekt. Helaas heeft het streven naar vrijgevigheid op het gebied van ethiek en het beschermen van patiënten ertoe geleid dat het financiële management van dat bedrijf zich ertoe heeft verbonden uitgebreid FDA-overtredingen en door rechters ervan beschuldigd te worden valse wetenschappelijke beweringen (wat allemaal toevallig gebeurde na mijn vertrek).
Zonder externe bevestiging van de kwaliteit van medicijnen zijn Amerikanen volledig afhankelijk van de FDA en fabrikanten om de zuiverheid van producten te beoordelen en te bevestigen. Er is aangetoond dat de veiligheid van geneesmiddelen een opmerkelijk probleem is als het gaat om Covid-mRNA-injecties. Helaas, als iemand zijn eigen analyse van mRNA-injecties wilde uitvoeren, dan was hij dat wel niet over een voldoende gedetailleerde ingrediëntenlijst beschikken om het mee te vergelijken, of zelfs toegang hebben tot de gevestigde regelgevingsmethodologie over hoe je het op de juiste manier kunt testen op zuiverheid.
Het komt omdat fabrikanten en de FDA houdt rekening met alle ingrediënten van deze mRNA-injecties, inclusief de sequentie van mRNA plus eigenschappen van lipide nanodeeltjes (LNP), inclusief halfwaardetijd, LNP-structuren, oppervlaktemodificatie(s), aantal/type(s) van LNP’s per dosis en bevestigingspunten op de mRNA-streng, niet gespecificeerd of ‘bedrijfsgeheim’.
Bovendien houdt de FDA ook rekening met de methodologieën over het testen van mRNA-injecties op zuiverheid is ook een bedrijfsgeheim.
Tweeledige steun en honderden miljarden belastinggeld, maar GEEN transparantie?
De mRNA-geheimhouding van Covid bestaat, ook al hadden zowel de regering-Trump als Biden volledige transparantie voorgesteld met mRNA-injecties, tot het punt waarop de intellectuele-eigendomsrechten van Covid-mRNA werden opgeheven. Desondanks staan zowel de FDA als de fabrikanten patenten, inclusief basisgegevens over deze injecties, toe als handelsgeheim. Ze doen dit ondanks dat alle fabrikanten van Covid-vaccins dit hebben ontvangen honderden miljoenen belastinggeld volgens Forbes/Statista publicaties.
Het bestuderen van de epidemiologie van de geneesmiddelenveiligheid is al moeilijk genoeg. Zonder verifieerbare productzuiverheid/consistentie is een volledige veiligheidsevaluatie onmogelijk.
Volledige transparantie van alle ingrediënten en kwaliteitscontrolemaatregelen zijn belangrijk, niet alleen omdat ze zwaar door de belastingbetaler werden gefinancierd met honderden miljoenen dollars, maar ook omdat er een hele reeks vragen zijn gerezen over de veiligheid en werkzaamheid van Covid-mRNA-injecties.
De goedkeuring ervan was niet alleen uitzonderlijk complex, maar werd daarna ook versneld door de toezichthouders minder dan een jaar. De meeste medicijnen en vaccins gaan doorgaans mee tien jaar om de veiligheid/werkzaamheid volledig te testen en te beoordelen en goed te keuren. Naast dat de ingrediënten volledig nieuw en zeer complex zijn, en de eerste in zijn soort die op grote schaal worden toegediend, is de ontwikkeling inclusief klinische veiligheids-/toxiciteitsbeoordelingen op lange termijn en epidemiologische beoordelingen werden versneld en waren waarschijnlijk niet volledig opgehelderd vóór de introductie.
FDA-ingrediëntverificatie, transparantie en ‘waarheidsgetrouwheid’ hebben precedenten die teruggaan tot de 1800e eeuw:
De analytische verificatie en de transparantie van ingrediënten of ‘waarheid in etikettering’ waar de inhoud van de fles zich bevindt nodig overeenkomen met de vermelde ingrediënten dateert van vóór de oprichting van de FDA, terug tot 1862. De huidige FDA is feitelijk ontstaan uit wat begon als een enkele medewerker van het ‘Department of Chemistry’, werkzaam bij het Amerikaanse ministerie van Landbouw.
Vervalsing, (gewijzigde of giftige ingrediënten) verkeerde merknaam (een vals etiket bevat of anderszins misleidend is, of onjuiste medische claims bevat), of verkeerde etikettering (bevat ingrediënten die niet op het productetiket staan vermeld) hebben allemaal een lange, lelijke geschiedenis gehad in Amerika. Er werd gedacht dat de flagrantheid zijn hoogtepunt had bereikt in het begin van de 19e eeuw – of in ieder geval toen het identificeerbaar werd – aangezien pas in 1862 technische processen waren ontwikkeld om fraude met ingrediënten te analyseren en op te sporen. Voordien zouden zogenaamde ‘reizende medicijnmannen’ die zichzelf ‘doktoren’ noemden (steevast met twijfelachtige of niet-bestaande geloofsbrieven) flessen met ‘genezende’ producten verkopen, waarvan de ingrediëntenlabels alleen vage of onschadelijke inhoud vermeldden, zoals “vitaminen""kruidenextracten,"Of"slangolie” – of hebben vaak helemaal geen ingrediëntenlijst.
Destijds waren er veel vrome, puriteinse New Englanders, die dat om religieuze redenen zouden doen nooit alcohol aanraken, zouden deze oplossingen van deze venters kopen en onbewust worden verleid tot het consumeren van oplossingen die niet alleen alcohol bevatten, maar ook verdovende middelen zoals opium en/of cocaïne. Onder het voorwendsel een belachelijk brede overvloed aan kwalen te verbeteren, ontwikkelden patiënten in plaats daarvan een bestraffende verslaving en/of werd hun gezondheid anderszins negatief beïnvloed door deze vroege ‘drugsdealers’.
Naarmate het probleem groeide, begon de federale overheid dit op te merken. Uiteindelijk werd de Pure Food and Drug Act werd aangenomen in 1906 en leidde tot de oprichting van de Food and Drug Administration (FDA).
[FDA had een formatief plicht om ervoor te zorgen dat medicijnen waarheidsgetrouwe etiketteringsverklaringen dragen en voldoen aan bepaalde normen voor zuiverheid en sterkte.
Vergeet niet dat hij bijna 120 jaar oud is waarheidsgetrouwe etiketteringsvereiste en het “zuiverheids”-gedeelte van de Pure Food and Drug Act van 1906, terwijl u verder leest over mRNA-verificatietests en transparantie van ingrediënten.]
Welke “waarheidsgetrouwe” en “zuivere” verificatietests voor ingrediënten vinden plaats voor door de FDA gereguleerde producten?
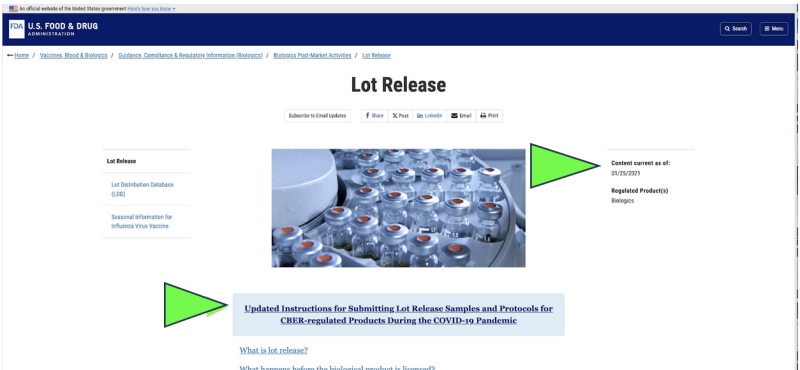
In 2021 koos de FDA ervoor om de farmaceutische kwaliteit van Amerika te gaan monitoren via een ophalen op afstand of per post verzonden monsters voor medicijnen als vervanging voor live-inspecties van faciliteiten vanwege de Covid-pandemie. Was dat legaal? Kan dat ooit als wetenschappelijk verantwoord worden beschouwd? Ondanks dat de pandemie voorbij is, worden momenteel de enige officiële testen op de vrijgave van farmaceutische producten uitgevoerd elke Covid mRNA farmaceutisch komt naar voren naar nog worden gedaan door de FDA via een door de fabrikant geleverde, “per post verzonden” monster volgens a screenshot van de huidige FDA-website. Het is duidelijk dat een “ingezonden” bemonsteringsmethode heel anders is en potentieel minder betrouwbaar dan het direct verzamelen van monsters via een directe, persoonlijke verzamelmethode. Desondanks beweert de FDA dat het “de hoogste standaard ter wereld voor bemonstering en testen. '
Bovendien stelt de FDA voor om haar “mail-in”-testbeleid op afstand verder te bevorderen met een nieuw voorgesteld richtsnoer.
Hoewel het alleen bestaat als een “concept” FDA-document, laten officiële FDA-websites dat zien het versturen van monsters lijkt al sinds januari 2021 te gebeuren. Het lijkt erop dat de FDA de resultaten van deze opgestuurde tests als hun onafhankelijke verificatie beweert.
Daarnaast worden de onderaan de eerste pagina van het FDA-concept document stelt uitbreiding van “testen op afstand” voor. Momenteel wordt vermeld elk FDA-productregulerende afdeling bij de FDA, wat impliceert dat het een beleidsvoorstel voor het hele agentschap is.
De volledige lijst omvat de:
- Bureau voor regelgevende zaken
- Bureau voor voedselbeleid en -respons
- Bureau voor combinatieproducten
- Centrum voor evaluatie en onderzoek van biologische geneesmiddelen
- Centrum voor geneesmiddelenevaluatie en -onderzoek
- Centrum voor Apparaten en Radiologische Gezondheid
- Centrum voor Voedselveiligheid en Toegepaste Voeding
- Centrum voor tabaksproducten
- Centrum voor Diergeneeskunde
Is “ingestuurde” kwaliteitscontrolebemonstering door de FDA geschikt? Wat als de restaurantinspecties van het Amerikaanse ministerie van Volksgezondheid het FDA-beleid zouden weerspiegelen?
Deze 'mail-in'-bemonsteringsmethode is net zo absurd als bijvoorbeeld een gezondheidsafdeling van een staat restaurants in de gaten houdt door hen te vragen periodiek verschillende items van hun menu naar een testfaciliteit te 'mailen', zodat gezondheidsafdelingen kunnen testen op mogelijk voedsel. -geboren besmetting, en/of restaurants vragen te beloven dat ze menu-items zelf zullen testen. Wat als dat restaurant in China was? Wat als dat restaurant in India was? Of welk ander land dan ook waarvan bekend is dat het een Erbarmelijke geschiedenis van fraude en kwaliteitscontrole problemen?
Deze methodologie zou onaanvaardbaar zijn voor zowel restaurants als farmaceutische bedrijven, om onder meer voor de hand liggende redenen: fabrikanten zouden de monsters kunnen insturen die zij verkiezen – niet noodzakelijkerwijs representatieve batchmonsters. Het is duidelijk niet hetzelfde als FDA-inspecteurs die monsters verzamelen tijdens onaangekondigde inspecties van de hele faciliteit.
Volgens de restaurant-analogie zouden alle restaurants dat natuurlijk doen monsters van klasse A indienen die niet noodzakelijkerwijs representatief zijn voor wat consumenten ontvangen.

Kwaliteitscontrole: wat is farmaceutische “vrijgavetest” en waarom is het belangrijk?
Tegenwoordig houdt de FDA toezicht op de kwaliteit en inhoud van $2.7 biljoen productwaarde per jaar, maar lijkt kritische beoordelingen en resultaten van ingrediëntenverificatie te onderdrukken. De FDA wordt verondersteld Amerikanen te beschermen door gedragsregels uit te voeren uitgebreid analytische tests als controlesom om de nauwkeurigheid van de ingrediënten te garanderen. De resultaten daarvan moeten transparant zijn voor de belastingbetalers die de financiering financieren FDA's $ 6.6 miljard begroting. Die wetenschappelijke verificatie wordt farmaceutische “vrijgave testen.” Releasetesten is een technische term die verwijst naar een proces dat een verscheidenheid aan instrumentele analyses omvat uitgebreid testproducten op zuiverheid, concentratie, consistentie, identiteit en onzuiverheden van welke aard dan ook.
De hele FDA is ontstaan uit die ene ‘Department of Chemistry’-medewerker uit 1862 en de behoefte aan transparantie en verificatie van ingrediënten. Tegenwoordig is die werknemer uitgegroeid tot een volledige FDA-afdeling van 1,300 wetenschappers en ondersteunend personeel vermoedelijk gewijd aan de verificatie van ingrediënten via het testen van farmaceutische vrijgave. Die van de FDA Bureau voor farmaceutische kwaliteit (OPQ) moet ervoor zorgen dat farmaceutische producten exact overeenkomen met de inhoud van de vermelde ingrediënten, zonder variatie in kwaliteit/onzuiverheid (kwalitatief) of inhoud (kwalitatief). De regels die dat vereisen, zijn zeer specifiek en gedetailleerd 21 CFR § 201.10.
Hoe de FDA mRNA-injecties verifieert voor kwaliteitscontrole:
De kwaliteitscontroleresultaten van tests met mRNA-injecties waren bijzonder kritisch omdat ze groot en complex zijn en snel werden uitgevoerd. Terwijl belastingbetalers afhankelijk zijn van de FDA voor het verifiëren van de kwaliteit van de mRNA-injectie en het delen van de resultaten, is de FDA afhankelijk van de FDA lijkt verplicht om de ingrediënten van fabrikanten te beschermen ten koste van zelfs de meest elementaire transparantie met betrekking tot mRNA Covid-producten. Hoewel de FDA monsters lijkt te verzamelen, is hun ‘mail-in’-methodologie fundamenteel gebrekkig. Bovendien deelt de FDA de resultaten van die tests nergens waar ik ze kan vinden.
Met andere woorden: tijdens de pandemie, toen gloednieuwe, breed geïmplementeerde mRNA-schoten met “warp-snelheid” op Amerikanen werden afgevuurd en toen Amerika het meest vertrouwde op de kwaliteits-/regelgevende taken van de FDA, accepteerde de FDA zelf ingediende “gemailde” in” kwaliteitscontroletests en/of resultaten. Heeft de FDA daar geen rekening mee gehouden mRNA-fabrikanten gaven toe dat ze ‘moeite [d]’ hadden om op de productie te reageren en dat ze ‘moesten’ om bij te blijven met productieprocessen? Fabrikanten van mRNA-ingrediënten verklaarden verder dat inspanningen om aan de behoeften te voldoen “ongekend” waren.
Uitspraken als deze wekken geen vertrouwen bij de consument in de kwaliteit en zijn illustratief voor de enorme opschaling van deze complexe producten die vooral waakzaam en persoonlijk FDA-onderzoek van faciliteiten en gefabriceerde producten, pandemie of niet. Eén fabrikant van mRNA-ingrediënten verklaarde bijvoorbeeld dat ze hun productie plotseling hadden opgevoerd 50 fold.
Te midden van die nieuwe technologie die met “warp speed” haast werd doorgedrukt, was geen van de 1,300 OPQ-wetenschappers bij de FDA die live inspecties eiste, of op zijn minst aanbood iets anders te doen dan te vragen om mogelijk twijfelachtige “ingezonden” monsters om uit te proberen?
De voor de hand liggende vraag is: waarom heeft de FDA niet rechtstreeks monsters verzameld? Zelfs nu de pandemie van kracht was, had de FDA faciliteiten kunnen inspecteren in beschermende pakken of – of op de zeer op zijn minst – kozen ervoor om monsters te verzamelen bij apotheken, ziekenhuizen of bij distributiemagazijnen.
Verborgen methodologie voor het testen van mRNA-injectie-ingrediënten:
Afgezien van het ontbreken van testresultaten en twijfelachtige “ingezonden” bemonsteringsresultaten – is de FDA dat wel bovendien het verbergen van hun gevalideerde methodologie waardoor anderen hun eigen, onafhankelijke analyses over de kwaliteit/zuiverheid van mRNA-injecties niet kunnen uitvoeren.
Het onafhankelijk analyseren van medicijnen op zuiverheid en potentiële besmetting in vergelijking met de ingrediëntenlijst is iets dat ik zelf had geprobeerd te doen toen ik 's werelds eerste analytische apotheek. Omdat mRNA-shots echter een nieuwe technologie zijn met een minder dan volledig transparante ingrediëntenlijst, is de testmethodologie die men zou moeten gebruiken niet eenvoudig, zoals bij andere geneesmiddelen met kleine moleculen. Iedereen die de opslag, stabiliteit, specificiteit, chemie, gevoeligheid of zelfs de basismethodologie voor het testen van validatie en/of resultaten probeert op te zoeken, wordt geblokkeerd via een FDA-rapport dat belachelijk invasieve redacties bevat, waardoor zelfs het meest fundamentele wetenschappelijke begrip ontstaat van hoe potentieel kan worden geëvalueerd resultaten of uitvoeringstesten onmogelijk.
Als aangrijpend visueel voorbeeld: een enkele geredigeerde pagina in een langere samenvatting van de FDA-regelgeving (hieronder weergegeven) maakt deel uit van een 127-pagina's tellende document (waarvan slechts 63 pagina’s zijn gedeeld, en van die 63 pagina’s is ongeveer 50% geredigeerd) over hoe de zuiverheid, concentratie en andere analytische maatregelen van mRNA-injecties kunnen worden geëvalueerd.
Die FDA (b)(4) redacties gespecificeerde gedetailleerde redacties gebruikt om “bedrijfsgeheimen en vertrouwelijke commerciële of financiële informatie beschermen.” Maar is het werkelijk gepast om het als ‘commercieel’ te bestempelen als het onderzoek/de ontwikkeling/het product ermee gefinancierd is? honderden miljoenen belastinggeld?

Zonder een lijst met ingrediënten of testmethodologie is het voor iemand anders buiten de FDA of fabrikanten onmogelijk om precies te weten hoe ze op producten moeten controleren. vervalsing (gewijzigde of giftige ingrediënten) of verkeerde etikettering (omdat een volledige lijst van ingrediënten, inclusief de nucleotidesequentie en de configuraties van lipide nanodeeltjes staan bijzonder vaag op het productetiket).
Het gebrek aan methodologie is vooral problematisch omdat nieuwe, voorlopige gegevens, waarbij gebruik wordt gemaakt van onafhankelijke methodologie, bewijs hebben geleverd DNA-besmetting bij mRNA Covid-injecties.
Dus als een extern individu beweert een onzuiverheid in mRNA-opnames te hebben getest en gevonden en de FDA of fabrikanten om hun reactie zou vragen, zouden ze een antwoord krijgen dat iets zegt in de trant van:
- U heeft geen gevalideerde/geschikte testmethodologie gebruikt om tot uw conclusies te komen en daarom zijn uw analyses ongeldig.
Daartoe zou het onafhankelijke laboratorium proberen de testmethodologie op te vragen uit door de FDA goedgekeurde documentatie (dat wil zeggen, het volledige document met daarin Figuur 5) door te vragen: “Oké, ik wil het graag testen met behulp van jouw goedgekeurde methodologie; Wil je ons vertellen wat dat is?”
- De FDA of de fabrikant zou iets antwoorden in de trant van: “Wat we bereid zijn bekend te maken over de gebruikte methodologie en dat niet vertrouwelijk is, kan online worden gevonden, of via een FDA FOIA-verzoek'...waar ze zouden worden opgewacht het volgende zwaar geredigeerde document, waar alles wat ook maar enigszins betekenisvol is, wordt bedekt met (b)(4)-redacties.
Tussen de regels door gelezen: het is duidelijk dat zowel de fabrikanten als de Amerikaanse FDA niet willen dat iemand anders dan zijzelf de volledige ingrediënten kent van mRNA-injecties of deze zelfs test op zuiverheid en consistentie.
Volgens FDA-functionarissen: farmaceutische productie wel Zeer Foutgevoelig:
Veel Er kunnen dingen misgaan – en dat gebeurt ook – tijdens het farmaceutische productieproces. Naast potentiële inconsistenties met mRNA/LNP-injecties zijn er ook kwalitatieve en kwantitatieve problemen elk FDA-gereguleerd farmaceutisch product. Zelfs het Huis en de Senaat hebben formeel de berichten erkend dat de FDA er niet in is geslaagd de Amerikaanse farmaceutische toeleveringsketen veilig te stellen. De meerderheid van Het Amerikaanse farmaceutische bedrijf consument-eindgebruikerproductEr wordt geproduceerd in het buitenland, in landen als India en China, en andere landen met lage arbeidskosten zijn dat wel niet staat bekend om zijn hoge kwaliteitscontrole. Het Federal Register staat vol met rapporten over overtredingen bij Indiase en Chinese fabrieken.
Certificeert de FDA deze fabrieken – inclusief die met een lange geschiedenis van overtredingen – ook via een “mail-in”-systeem naar de FDA? Schandalig genoeg is het antwoord op de vraag iets waar iedereen die zich met farmaceutische kwaliteit bezighoudt zich zeer ongemakkelijk bij zou voelen.
Terwijl een Six Sigma Het precisieniveau is lange tijd het doel geweest voor kwaliteit en veiligheid in de auto-, computer-, mobiele telefoon- en andere hightech-productiesectoren, maar lijkt grotendeels over het hoofd te zijn gezien als het gaat om de farmaceutische productie.
FDA-functionarissen hebben gegevens gepubliceerd die een schatting maken van 2-3σ (sigma) onnauwkeurigheid in de farmaceutische productie. Een 2σ-kwaliteit komt overeen met 308,537 defecten per 1,000,000 mogelijkheden. (Er zijn waarschijnlijk veel meer dan 1,000,000 kansen op fouten als het gaat om de farmaceutische productie.) De FDA is zich hiervan bewust op de hoogste niveaus van leiderschap; in feite de huidige FDA-hoofd van het Office of Pharmaceutical Quality, Michael Kopcha schreef en publiceerde zelfs de bovenstaande Six Sigma-berekening, waarbij hij de onnauwkeurige aard van de farmaceutische productie betreurde weer 2017.
De foutmarge voor mRNA-producten en/of hun LNP's zou gelijk kunnen zijn minder nauwkeuriger dan de 2-3σ (hoe lager de σ, hoe onjuister een product is) omdat ze nucleotidemateriaal en nieuwe LNP’s bevatten, waardoor ze substantieel complexer zijn dan farmaceutische producten met kleine moleculen – ondanks dat ze worden ontwikkeld, geproduceerd en uitgebracht op “ Warp snelheid."
Nu zelfs de FDA en haar functionarissen een inherente onnauwkeurigheid bij de productie erkennen, waarom in de wijde sportwereld Vervult de FDA haar veiligheidsmissie niet door haar vrijgavetests van mRNA-technologie publiekelijk te delen met het Amerikaanse publiek dat ze financiert?
Opnieuw vóór 1862? Zijn mRNA-shots de enige medicijnen waarvoor Amerikanen niet beschikken? Volledige Ingrediëntinformatie?
Het gebrek aan duidelijkheid over het aantal sequenties van mRNA-opnamen en andere kritische informatie staat in direct contrast met een ander door de FDA goedgekeurd RNA-gebaseerd medicijn – patisiran (Onpattro®). Onpattro verstrekt op transparante wijze de volgorde, het molecuulgewicht en de milligramsterkte van zijn producten binnen de officiële FDA pakket etikettering zoals geïllustreerd in een fragment hieronder:


Gebrek aan Covid-mRNA Dosisspecificiteit: 0.3 ml (of 0.5 ml) van wat?
Op dit moment hebben we nog steeds geen basisinformatie over de ingrediënten van welke Covid-mRNA-injectie dan ook. Apothekers weten alleen een specifiek te geven volume van vloeistof, en deed dit schijnbaar zonder twijfel. Normaal gesproken zou de officiële FDA-verpakkingsetikettering de werkelijke ingrediënten in dat volume moeten vermelden, maar niet voor Covid-mRNA-etiketten: ze vermelden eenvoudigweg 0.3 ml (of 0.5 ml) als de ‘Doseringsvorm en sterkte’.
Bovendien is 0.3/0.5 ml, zoals elke middelbare scholier je kan vertellen, een volume, niet een sterkte. We kennen geen kwantitatieve details van wat er in die 0.3/0.5 ml zit, zoals: Hoeveel LNP-deeltjes? Welke grootte/morfologieën van die LNP's? Hoeveel mRNA-sequenties in dat volume?




Is dit wat door de FDA wordt beschouwd als voldoende transparant of als ‘waarheidsgetrouwe etikettering’?
Het bovenstaande knip-en-plakfragment uit de bijsluiter is alle informatie die fabrikanten delen met consumenten over de dosis – die jammerlijk ontoereikend is in vergelijking met alle andere FDA-labels – of iedereen die nieuwsgierig is naar iets anders dan hoeveel vloeistof te injecteren en de concentratie van 30 of 100 mcg van een niet-gespecificeerde mRNA-sequentie.
De opmerkelijke onnauwkeurigheid van dit label, toegestaan door de FDA, lijkt specifiek in strijd te zijn met het bijna 120 jaar oude label: “eisen dat voedsel en medicijnen waarheidsgetrouwe etiketteringsverklaringen dragen en aan bepaalde normen voor zuiverheid en sterkte voldoen. '
Is dit wat door de FDA wordt doorgegeven als een “waarheidsgetrouwe” lijst met ingrediënten? (Zien 21CFR §352 en 21 CFR §201.10 met betrekking tot “verklaring van ingrediënten” en “medicijnen en apparaten met een verkeerd merk.”)
De vraag is: worden er onbekende of niet-specifieke ingrediënten vermeld die niemand behalve de fabrikant kan ontcijferen? werkelijk voldoen aan de geest of wettelijke eisen van “labeling?” Is dat label wat door de Amerikaanse FDA als ‘waarheidsgetrouw’ wordt beschouwd? Aan wiens kant staat de FDA eigenlijk; fabrikanten of consumenten?
Behalve dat het niet direct wordt gespecificeerd, kan het exacte aantal LNP- of mRNA-strengen in een injectie van 30 of 100 mcg niet eens worden geëxtrapoleerd stoichiometrisch of op basis van Avogadro's nummer, omdat de mRNA-sequentie, het molecuulgewicht en/of de LNP-component/-configuraties nergens binnen de officiële FDA-labeling worden vermeld.
Hoe kan iemand weten of het aantal mRNA-strengen dat voor het spike-eiwit voor Covid codeert, evenredig is aan de hoeveelheid Covid-inoculum die iemand zou krijgen als gevolg van een door de gemeenschap opgelopen infectie? Antwoord: ze kunnen niet.
Zijn Covid-mRNA-injecties Correct geëtiketteerd/verkeerd geëtiketteerd?
21 CFR 211.125 specificeert “Er zal strikte controle worden uitgeoefend op de etikettering die wordt afgegeven voor gebruik bij de etikettering van geneesmiddelen.'Maar het lijkt erop dat de FDA ondanks het feit zo laks was met de goedgekeurde etikettering van Covid-mRNA-injecties elk ander medicijn – inclusief het op mRNA gebaseerde Onpattro – specificeert die informatie wel. Historisch gezien zijn de regelgevende beslissingen van de FDA (zoals welke informatie moet worden opgenomen in de etikettering van producten) gebaseerd op voorrang, en waren mRNA-opnamen van Covid een duidelijke afwijking van de historische en juridische voorrang van de FDA. Die opmerkelijke afwezigheid van gegevens en gebrek aan duidelijkheid grijpt terug op de dagen van Morley's lever- en nierhart aan het eind van de 1800e eeuw. Het verschil is: toen bestond de FDA nog niet, maar vandaag de dag is er een FDA met ongeveer 20,000 werknemers, van wie sommigen ogenschijnlijk geloofden dat dit label transparant en ‘waarheidsgetrouw’ was.
Het vermelden van een onbekend/niet te ontcijferen/obscur ingrediënt dat niemand ooit nauwkeurig zou kunnen bepalen, is niet wat de wetgevers van de Pure Food and Drug Act uit 1906 bedoelden toen ze de FDA-regels over ‘waarheidsgetrouwe etikettering’ specificeerden. Los daarvan: het feit dat de doses per volume van verschillende fabrikanten worden verdubbeld (30 mcg/0.3 ml vs 100 mcg/0.5 ml) betekent dat deze mRNA-sequenties enorm verschillend lijken te zijn wat betreft nucleotidelengte, en dat op hun beurt ook zouden zijn meer en verschillende LNP's plus bijlagen. Betekent dit dat de mRNA-sequenties die worden gebruikt om het spike-eiwit te transcriberen ongeveer twee keer zo groot zijn (10 mcg/0.1 ml versus 20 mcg/0.1 ml) in vergelijking met andere fabrikanten, of draagt iets anders bij aan het verschil in nucleotidelengte?
Voor de leek die tot nu toe nog aan het lezen is (een pluim trouwens): het ontbreken van gedetailleerde etiketteringsinformatie kan hetzelfde zijn als het in grote lijnen adverteren voor een huis dat te koop staat, waarbij wordt gezegd dat het is gemaakt van hout en baksteen, op een cementplaat – maar dat wordt niet weergegeven. eventuele foto's van het huis (bijvoorbeeld de volgorde) en het niet delen van de vierkante meters (bijvoorbeeld het molecuulgewicht). Hoe dan ook is het gebrek aan informatie ontoereikend en een afwijking van traditionele normen.
Elk ander door de FDA goedgekeurd medicijn – inclusief andere mRNA-medicijnen – bevat volledige informatie over de ingrediënten op hun producten, inclusief een structurele weergave en molecuulgewicht van hun product, zodat mensen precies weten wat ze krijgen.
Het is waar: zoek het medicijn op dat je maar kunt bedenken in de Drugs.com-database en merk op hoe alle labels structuur en/of molecuulgewicht bieden. Bewijs dat Covid-mRNA-injecties een opvallend uitzondering op de historische goedkeuringspraktijk van de FDA en de ‘waarheidsgetrouwe etikettering’-regel.
Deens onderzoek uit 2023 beschrijft significante klinische variabiliteit tussen batches mRNA Covid-19 mRNA-injecties:
Het ontbreken van enige transparantie over zelfs mogelijk ongeldige “ingestuurde” testvalidaties lijkt fabrikanten een ander cruciaal belangrijk onderdeel te hebben gegeven van waar de FDA toezicht op houdt: mogelijke klinische manifestaties bij lot-/batchvariaties van mRNA-opnamen. Een terugblik Deense veiligheidsstudie eerder in 2023 gepubliceerd, werd een zeer afwijkend patroon beschreven van meldingen van bijwerkingen van de Pfizer-BioNTech BNT162b2 mRNA-injecties, zoals gecorreleerd met het Deense DKMA-rapportagesysteem voor bijwerkingen.
In de lijngrafiek die volgt, vertegenwoordigen verschillende gekleurde stippen verschillende batches mRNA-injecties van Pfizer-BioNTech. Het verdeelde batches in drie verschillende categorieën; hoog-laag- tot (bijna) afwezig aantal gerapporteerde groepen met bijwerkingen (respectievelijk blauwe, groene en gele grafieken).
Met andere woorden: Vermeend “equivalente” producten van dezelfde fabrikant lijken een enorm verschillende incidentie van bijwerkingen te hebben, per batch, waarbij elk van die batches honderdduizenden mRNA-injecties vertegenwoordigt.
Toen overeenkomstige lineaire regressielijnen werden toegevoegd, ontstond een bepaald patroon:
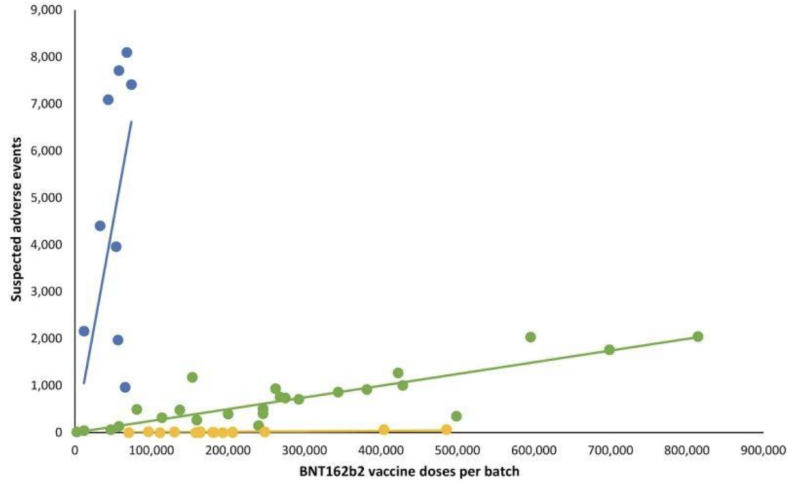
Belangrijke vragen over de opmerkelijke verschillen in bijwerkingen tussen mRNA-batches van Covid-19 zijn onder meer:
- Kunnen varianties van bijwerkingen het gevolg zijn van kwalitatieve of kwantitatieve varianties in mRNA-sequenties of het aantal mRNA-strengen tussen batches?
- Kunnen afwijkingen in ongewenste gebeurtenissen te wijten zijn aan kwalitatieve of kwantitatieve verschillen in de grootte/morfologie of hoeveelheid van LNP's tussen batches? Welke tests zijn er uitgevoerd de veiligheid van verschillende LNP's garanderen gebruikt bij mRNA-injecties?
- Waren de batches die overeenkwamen met de gele versus groene versus blauwe datapunten op de een of andere manier kwalitatief of kwantitatief verschillend?
- Kwam de opslag/hantering na de productie in de toedieningsfaciliteit (of ergens anders in de toeleveringsketen) in gevaar, wat leidde tot productvariabiliteit?
- Wat is het Sigma/foutenpercentage van deze en andere producten die afkomstig zijn van de specifieke productiefaciliteit/ploegchef die verantwoordelijk is voor de productie?
- Waren de ingrediënten van deze mRNA-producten van Covid afkomstig uit India of China of elders, afhankelijk van de batch?
- Welke percentages batches van Covid-mRNA-producten zijn getest via persoonlijke verzameling door een FDA-inspecteur, in plaats van dat ze vanaf het begin tot nu toe zijn ‘opgestuurd’? Werd elke batch getest met slechts een van deze twee verzamelmethoden?
- Heeft de FDA een vrijgavetestverificatie uitgevoerd op de Deense partijen van het DKMA-rapportagesysteem voor ongewenste voorvallen? Zo ja, waarom geeft de FDA deze specifieke testresultaten niet vrij? Zo nee, waarom zijn er geen tests uitgevoerd?
- Bestaat er een fundamenteel probleem bij het consistent en betrouwbaar en zonder contaminatie produceren van LNP's en/of mRNA-sequenties?
De resultaten van het Deense onderzoek en de bovenstaande vragen over bijwerkingen kunnen *beginnen* te worden beantwoord, maar niet zonder dat de FDA onafhankelijk de resultaten van hun vrijgavetestresultaten deelt. Zoals het er nu uitziet, kent niemand vanwege de alomtegenwoordige FDA (b)(4)-redacties de gevalideerde methodologie voor het testen van Covid-mRNA-opnamen or welke partijen in het Deense onderzoek precies wel of niet zijn getest or de resultaten van die batchtests.
…Maar zelfs als de FDA ervoor had gekozen om die batchtestresultaten vrij te geven, hoe weten consumenten dan of die resultaten representatief zijn voor de gespecificeerde batches, aangezien fabrikanten zelf selecteren welke monsters ze ‘opsturen’?
Het niet bieden van transparantie over ingrediënten en het garanderen van de kwaliteit via een geschikte bemonsteringsmethode is een fundamentele en basisvereiste van de FDA. In feite was dit de belangrijkste reden voor de oprichting van de FDA! Verdienen Amerikanen geen betere wetten op het gebied van transparantie, toezicht en ‘waarheidsgetrouwe etikettering’ als het gaat om onze farmaceutische producten – vooral omdat die wetten meer dan 100 jaar geleden zijn gemaakt?
Uitgegeven onder a Creative Commons Naamsvermelding 4.0 Internationale licentie
Stel voor herdrukken de canonieke link terug naar het origineel Brownstone Instituut Artikel en auteur.









