Aangezien sommige mensen nu al meer dan een half jaar zijn gevaccineerd, stromen er bewijzen binnen over de werkzaamheid van het Covid-vaccin. De gestalt van de bevindingen impliceert dat de infectie-explosie die we wereldwijd hebben ervaren – na dubbele vaccinatie in bijvoorbeeld Israël, het VK, de VS enz. – te wijten kan zijn aan het feit dat de gevaccineerde Covid evenveel of meer verspreidt dan de niet-gevaccineerde.
Een voor de hand liggende vraag is of vaccins met een beperkte capaciteit om symptomatische ziekten te voorkomen de evolutie van meer virulente stammen kunnen stimuleren? In een PLoS-biologie dit artikel uit 2015, Read et al. geconstateerd dat:
"Conventionele wijsheid is dat natuurlijke selectie zeer dodelijke ziekteverwekkers zal verwijderen als de dood van de gastheer de overdracht aanzienlijk vermindert. Vaccins die gastheren in leven houden maar toch overdracht mogelijk maken, kunnen er dus voor zorgen dat zeer virulente stammen in een populatie kunnen circuleren."
Dus in plaats van dat de niet-gevaccineerden de gevaccineerden in gevaar brengen, zouden het in theorie de gevaccineerden kunnen zijn die de niet-gevaccineerden in gevaar brengen.
Hier vat ik onderzoeken en rapporten samen die licht werpen op de door vaccins geïnduceerde immuniteit tegen Covid. Ze benadrukken de problemen met vaccinmandaten die momenteel de banen van miljoenen mensen bedreigen. Ook stellen ze vraagtekens bij de argumenten voor het vaccineren van kinderen.
| 1) Gazit et al | toonde aan dat “SARS-CoV-2-naïeve gevaccineerden een 13-voudig (95% BI, 8-21) verhoogd risico hadden op doorbraakinfectie met de Delta-variant in vergelijking met degenen die eerder geïnfecteerd waren.” Bij correctie voor het tijdstip van ziekte/vaccinatie was er een 27-voudig verhoogd risico (95% BI, 13-57). |
| 2) Acharya et al. | Het risico op infectie negeren, gezien het feit dat iemand besmet was, Acharya et al. vonden "geen significant verschil in cyclusdrempelwaarden tussen gevaccineerde en niet-gevaccineerde, asymptomatische en symptomatische groepen die zijn geïnfecteerd met SARS-CoV-2 Delta." |
| 3) Riemersma et al. | vonden “geen verschil in virale belasting bij het vergelijken van niet-gevaccineerde personen met degenen die vaccin-“doorbraak”-infecties hebben. Bovendien testen personen met doorbraakinfecties door vaccins vaak positief met virale ladingen die consistent zijn met het vermogen om besmettelijke virussen te verspreiden." De resultaten geven aan dat “als gevaccineerde personen besmet raken met de deltavariant, zij bronnen van SARS-CoV-2-overdracht naar anderen kunnen zijn.” Ze rapporteerden “lage Ct-waarden (<25) bij 212 van de 310 volledig gevaccineerde (68%) en 246 van de 389 (63%) niet-gevaccineerde personen. Het testen van een subset van deze monsters met een lage Ct onthulde besmettelijke SARS-CoV-2 in 15 van de 17 exemplaren (88%) van niet-gevaccineerde personen en 37 van de 39 (95%) van gevaccineerde personen.” |
| 4) Chematelly et al. | In een studie uit Qatar, Chematelly et al. gerapporteerde werkzaamheid van het vaccin (Pfizer) tegen ernstige en dodelijke ziekte, met een werkzaamheid in het bereik van 85-95% ten minste tot 24 weken na de tweede dosis. Daarentegen nam de werkzaamheid tegen infectie af tot ongeveer 30% 15-19 weken na de tweede dosis. |
| 5) Riemersma et al. | Riemersma et al. uit Wisconsin. meldde dat gevaccineerde personen die besmet raken met de Delta-variant SARS-CoV-2 op anderen kunnen overdragen. Ze vonden een verhoogde viral load bij de niet-gevaccineerde en gevaccineerde symptomatische personen (respectievelijk 68% en 69%, 158/232 en 156/225). Bovendien ontdekten ze bij de asymptomatische personen verhoogde virale lasten (respectievelijk 29% en 82%) bij respectievelijk de niet-gevaccineerden en de gevaccineerden. Dit suggereert dat de gevaccineerden het virus gemakkelijk en onbewust kunnen besmetten, herbergen, cultiveren en overdragen. |
| 6) Subramanian | Subramanian meldde dat “er op landelijk niveau geen waarneembaar verband lijkt te bestaan tussen het percentage van de bevolking dat volledig is gevaccineerd en nieuwe COVID-19-gevallen.” Bij het vergelijken van 2947 provincies in de Verenigde Staten waren er iets minder gevallen op meer gevaccineerde locaties. Met andere woorden, er is geen duidelijk waarneembaar verband. |
| 7) Chau et al. | gekeken naar de overdracht van de SARS-CoV-2 Delta-variant onder gevaccineerde gezondheidswerkers in Vietnam. Van de 69 gezondheidswerkers die positief testten op SARS-CoV-2, namen er 62 deel aan de klinische studie, die allemaal herstelden. Van 23 daarvan werden volledige genoomsequenties verkregen, die allemaal tot de Delta-variant behoorden. “De virale belasting van doorbraakgevallen met Delta-variantinfecties was 251 keer hoger dan die van gevallen die tussen maart en april 2020 met oude stammen waren geïnfecteerd”. |
| 8) Bruin et al. | In Barnstable, Massachusetts, Brown et al. ontdekte dat van de 469 gevallen van COVID-19 74% volledig was gevaccineerd en dat “de gevaccineerden gemiddeld meer virus in hun neus hadden dan de niet-gevaccineerden die besmet waren.” |
| 9) Hetemäli et al. | Rapporteren over een nosocomiale ziekenhuisuitbraak in Finland, Hetemäli et al. merkte op dat "zowel symptomatische als asymptomatische infecties werden gevonden onder gevaccineerde gezondheidswerkers, en secundaire overdracht vond plaats van degenen met symptomatische infecties ondanks het gebruik van persoonlijke beschermingsmiddelen." |
| 10) Shirit et al. | In een ziekenhuis uitbraak onderzoek in Israël, Shitrit et al. waargenomen "hoge overdraagbaarheid van de SARS-CoV-2 Delta-variant onder tweemaal gevaccineerde en gemaskerde personen." Ze voegden eraan toe dat "dit suggereert dat de immuniteit enigszins afneemt, hoewel het nog steeds bescherming biedt aan personen zonder comorbiditeit." |
| 11) UK COVID-19-vaccin Surveillance Report voor week #42 | In het UK COVID-19-vaccin Surveillance Report voor week #42, werd opgemerkt dat er sprake is van "afname van de N-antilichaamrespons na verloop van tijd" en "dat N-antilichaamniveaus lager lijken te zijn bij personen die een infectie oplopen na 2 vaccinaties." Uit hetzelfde rapport (Tabel 2, pagina 13) blijkt dat in de oudere leeftijdsgroepen boven de 30, de dubbel gevaccineerde personen een groter infectierisico hebben dan de niet-gevaccineerde, vermoedelijk omdat de laatste groep meer mensen omvat met een sterkere natuurlijke immuniteit tegen eerdere Covid-ziekte. Daarentegen hadden de gevaccineerde mensen een lager risico op overlijden dan de niet-gevaccineerde, in alle leeftijdsgroepen, wat aangeeft dat vaccins meer bescherming bieden tegen overlijden dan tegen infectie. Zie ook UK PHE-rapporten 43, 44, 45, 46 voor vergelijkbare gegevens. |
| 12) Levin et al. | In Israël, Levin et al. "voerde een 6 maanden durend longitudinaal prospectief onderzoek uit met gevaccineerde gezondheidswerkers die maandelijks werden getest op de aanwezigheid van anti-spike IgG en neutraliserende antilichamen". Ze ontdekten dat "zes maanden na ontvangst van de tweede dosis van het BNT162b2-vaccin de humorale respons aanzienlijk was afgenomen, vooral bij mannen, bij personen van 65 jaar of ouder en bij personen met immunosuppressie." |
| 13) Rosenberg et al. | In een studie uit de staat New York, Rosenberg et al. rapporteerde dat “Tijdens 3 mei – 25 juli 2021, was de totale, voor leeftijd gecorrigeerde vaccineffectiviteit tegen ziekenhuisopname in New York relatief stabiel 89.5%–95.1%). De totale voor leeftijd gecorrigeerde vaccineffectiviteit tegen infectie voor alle volwassenen in New York daalde van 91.8% naar 75.0%.” |
| 14) Sutar et al. | Sutar et al. merkte op dat “Onze gegevens een aanzienlijke afname van antilichaamresponsen en T-celimmuniteit tegen SARS-CoV-2 en zijn varianten aantonen, 6 maanden na de tweede immunisatie met het BNT162b2-vaccin.” |
| 15) Nordstrom et al. | In een studie van de Universiteit van Umeå in Zweden, Nordstrom et al. merkte op dat “de vaccineffectiviteit van BNT162b2 tegen infectie geleidelijk afnam van 92% (95% BI, 92-93, P<0) op dag 001-15 tot 30% (47% BI, 95-39, P<55· 0) op dag 001-121, en vanaf dag 180 en daarna kon geen effectiviteit worden gedetecteerd (211%; 23% BI, -95-2, P=41).” |
| 16) Jahi et al. | Jahi et al. hebben gemeld dat “in het geval van de Delta-variant neutraliserende antilichamen een verminderde affiniteit hebben voor het spike-eiwit, terwijl faciliterende antilichamen een opvallend verhoogde affiniteit vertonen. Antilichaamafhankelijke versterking kan dus een punt van zorg zijn voor mensen die vaccins krijgen op basis van de oorspronkelijke pieksequentie van de Wuhan-stam." |
| 17) Goldberg et al. | (BNT162b2-vaccin in Israël) meldde dat “de immuniteit tegen de delta-variant van SARS-CoV-2 een paar maanden na ontvangst van de tweede dosis vaccin in alle leeftijdsgroepen afnam.” |
| 18) Singanayagam et al. | onderzocht de overdracht en de kinetiek van de virale belasting bij gevaccineerde en niet-gevaccineerde personen met milde deltavariantinfectie in de gemeenschap. Ze ontdekten dat (in 602 gemeenschapscontacten (geïdentificeerd via het Britse contractopsporingssysteem) van 471 Britse COVID-19-indexgevallen werden gerekruteerd voor de beoordeling van overdracht en besmettelijkheid van COVID-19 in de cohortstudie van Contacten en 8145 monsters van de bovenste luchtwegen bijdroegen van dagelijkse bemonstering gedurende maximaal 20 dagen) “vaccinatie vermindert het risico op deltavariantinfectie en versnelt de virale klaring. Desalniettemin hebben volledig gevaccineerde personen met doorbraakinfecties een maximale virale belasting die vergelijkbaar is met niet-gevaccineerde gevallen en kunnen ze efficiënt infectie overbrengen in huishoudelijke omgevingen, ook naar volledig gevaccineerde contacten.” |
| 19) Keehner et al. | in NEJM, heeft onlangs gerapporteerd over de heropleving van SARS-CoV-2-infectie in een sterk gevaccineerd personeelsbestand in de gezondheidszorg. Vaccinatie met mRNA-vaccins begon medio december 2020; in maart was 76% van de beroepsbevolking volledig gevaccineerd en in juli was dit percentage gestegen tot 87%. Infecties waren begin februari 2021 dramatisch afgenomen…”samenvallend met het einde van het maskermandaat van Californië op 15 juni en de snelle dominantie van de B.1.617.2 (delta) variant die medio april voor het eerst opdook en goed was voor meer dan 95% van de UCSDH-isolaten tegen het einde van juli, infecties namen snel toe, inclusief gevallen onder volledig gevaccineerde personen … onderzoekers meldden dat de “dramatische verandering in de effectiviteit van het vaccin van juni tot juli waarschijnlijk te wijten is aan zowel de opkomst van de delta-variant als de afnemende immuniteit over tijd." |
| 20) Juthani et al. | Juthani et al. probeerde de impact van vaccinatie op opname in het ziekenhuis te beschrijven bij patiënten met een bevestigde SARS-CoV-2-infectie met behulp van real-world gegevens verzameld door het Yale New Haven Health System. “Patiënten werden als volledig gevaccineerd beschouwd als de laatste dosis (ofwel de tweede dosis van BNT162b2 of mRNA-1273, of de eerste dosis van Ad.26.COV2.S) ten minste 14 dagen vóór het begin van de symptomen werd toegediend of een positieve PCR-test voor SARS- CoV-2. In totaal identificeerden we 969 patiënten die werden opgenomen in een Yale New Haven Health System-ziekenhuis met een bevestigde positieve PCR-test voor SARS-CoV-2. BNT162b2-vaccin dan bij degenen die mRNA-1273 of Ad.26.COV2.S kregen…” |
| 21) de CDC | Een zeer recente studie gepubliceerd door de CDC meldde dat een meerderheid (53%) van de patiënten die in het ziekenhuis waren opgenomen met Covid-19-achtige ziekten al volledig waren gevaccineerd met RNA-injecties met twee doses. Tabel 1 laat zien dat van de 20,101 immuungecompromitteerde volwassenen die met Covid-19 in het ziekenhuis waren opgenomen, 10,564 (53%) volledig waren gevaccineerd met het Pfizer- of Moderna-vaccin (vaccinatie werd gedefinieerd als het ontvangen van precies 2 doses van een op mRNA gebaseerd COVID-19-vaccin ≥ 14 dagen vóór de indexdatum van de ziekenhuisopname, de datum van het verzamelen van respiratoire monsters in verband met het meest recente positieve of negatieve SARS-CoV-2-testresultaat vóór de ziekenhuisopname of de ziekenhuisopnamedatum als de test pas na de opname plaatsvond). Dit benadrukt de voortdurende uitdagingen waarmee Delta doorbreekt bij vaccinatie. |
| 22) Eyré, 2021 De impact van SARS-CoV-2-vaccinatie op de overdracht van alfa- en deltavarianten. | Eyre, 2021 keek naar de impact van SARS-CoV-2-vaccinatie op de overdracht van alfa- en deltavarianten. Ze meldden dat “hoewel vaccinatie het risico op infectie nog steeds verlaagt, vergelijkbare virale ladingen bij gevaccineerde en niet-gevaccineerde personen die besmet zijn met Delta zich afvragen hoeveel vaccinatie verdere overdracht verhindert... transmissiereducties daalden in de loop van de tijd sinds de tweede vaccinatie, want Delta bereikte vergelijkbare niveaus als niet-gevaccineerde personen door 12 weken voor ChAdOx1 en aanzienlijk verzwakkend voor BNT162b2. Bescherming tegen vaccinatie bij contacten nam ook af in de 3 maanden na de tweede vaccinatie … vaccinatie vermindert de overdracht van Delta, maar minder dan de Alpha-variant. |
| 23) Levine-Tiefenbrun | Levine-Tiefenbrun, 2021 bekeken Virale ladingen van Delta-variant SARS-CoV-2 doorbraakinfecties na vaccinatie en booster met BNT162b2, en rapporteerde dat de effectiviteit van de vermindering van de virale belasting met de tijd na vaccinatie afneemt, "aanzienlijk afneemt na 3 maanden na vaccinatie en effectief verdwijnt na ongeveer 6 maanden." |
| 24) Puranik, 2021 Vergelijking van twee zeer effectieve mRNA-vaccins voor COVID-19 tijdens perioden van prevalentie van Alpha- en Delta-varianten | Puranik, 2021 keek naar een Vergelijking van twee zeer effectieve mRNA-vaccins voor COVID-19 tijdens perioden van prevalentie van Alpha- en Delta-varianten, rapporterend: "In juli is de effectiviteit van vaccins tegen ziekenhuisopname hoog gebleven (mRNA-1273: 81%, 95% BI: 33-96.3%; BNT162b2: 75%, 95% BI: 24-93.9%), maar de effectiviteit tegen infectie was lager voor beide vaccins (mRNA-1273: 76%, 95% BI: 58–87%; BNT162b2: 42%, 95% BI: 13–62%), met een meer uitgesproken verlaging voor BNT162b2.” |
| 25) Saade, 2021 Testen op neutralisatie van levende virussen bij herstellende patiënten en proefpersonen die zijn gevaccineerd tegen 19A-, 20B-, 20I/501Y.V1- en 20H/501Y.V2-isolaten van SARS-CoV-2 | Saade, 2021 bekeken Testen op neutralisatie van levende virussen bij herstellende patiënten en proefpersonen die zijn gevaccineerd tegen 19A-, 20B-, 20I/501Y.V1- en 20H/501Y.V2-isolaten van SARS-CoV-2, en gerapporteerd als "Beoordeeld het neutraliserende vermogen van antilichamen om celinfectie te voorkomen, met behulp van een levende virusneutralisatietest met verschillende stammen [19A (eerste), 20B (B.1.1.241-afstamming), 20I/501Y.V1 (B. 1.1.7 afstamming) en 20H/501Y.V2 (B.1.351 afstamming)] in serummonsters verzameld uit verschillende populaties: twee doses gevaccineerde COVID-19-naïeve gezondheidswerkers (HCW's; Pfizer-BioNTech BNT161b2), 6 maanden post milde COVID-19 HCW's en kritieke COVID-19-patiënten... de bevinding van de huidige studie is de verminderde neutraliserende respons die is waargenomen tegen de 20H/501Y.V2-variant bij volledig geïmmuniseerde personen met het BNT162b2-vaccin in vergelijking met het wildtype en 20I/ 501Y.V1-variant.” |
| 26) Canada, 2021 Aanzienlijke vermindering van humorale immuniteit bij gezondheidswerkers en verpleeghuisbewoners 6 maanden na COVID-19 BNT162b2 mRNA-vaccinatie | Canaday, 2021 bekeken Aanzienlijke vermindering van humorale immuniteit bij gezondheidswerkers en verpleeghuisbewoners 6 maanden na COVID-19 BNT162b2 mRNA-vaccinatie, rapporterend: "Anti-spike, anti-RBD en neutralisatieniveaus daalden met meer dan 84% gedurende 6 maanden in alle groepen, ongeacht eerdere SARS-CoV-2-infectie. Zes maanden na vaccinatie had 6% van de infectie-naïeve NH-bewoners neutralisatietiters op of onder de ondergrens van detectie vergeleken met 70% 16 weken na volledige vaccinatie. Deze gegevens tonen een significante verlaging van de niveaus van antilichaam in alle groepen aan. Vooral die infectie-naïeve NH-bewoners hadden onmiddellijk een lagere humorale immuniteit na vaccinatie en vertoonden de grootste dalingen 2 maanden later.” |
| 27) Israël, 2021 Grootschalig onderzoek naar het verval van antilichaamtiter na BNT162b2-mRNA-vaccin of SARS-CoV-2-infectie | Israël, 2021 bekeken Grootschalig onderzoek naar het verval van antilichaamtiter na BNT162b2-mRNA-vaccin of SARS-CoV-2-infectie, en gerapporteerd als "Om de kinetiek van SARS-CoV-2 IgG-antilichamen te bepalen na toediening van twee doses BNT162b2-vaccin of SARS-CoV-2-infectie bij niet-gevaccineerde personen ... Bij gevaccineerde personen daalden de antilichaamtiters met elk tot 40% volgende maand, terwijl ze in revalidanten met minder dan 5% per maand afnamen. Zes maanden na BNT162b2-vaccinatie had 16.1% van de proefpersonen antilichaamspiegels onder de seropositiviteitsdrempel van <50 AU/ml, terwijl slechts 10.8% van de herstellende patiënten onder de drempel van <50 AU/ml lag na 9 maanden van SARS-CoV-2-infectie. ” |
| 28) Eyran, 2020 De longitudinale kinetiek van antilichamen bij COVID-19 herstelde patiënten ouder dan 14 maanden | Eyran, 2020 onderzocht De longitudinale kinetiek van antilichamen bij COVID-19 herstelde patiënten ouder dan 14 maanden, en vonden “een significant sneller verval bij naïeve gevaccineerden in vergelijking met herstelde patiënten, wat suggereert dat het serologische geheugen na natuurlijke infectie robuuster is in vergelijking met vaccinatie. Onze gegevens benadrukken de verschillen tussen serologisch geheugen veroorzaakt door natuurlijke infectie versus vaccinatie." |
| 29) Salvatore et al. | Salvatore et al. onderzocht het transmissiepotentieel van gevaccineerde en niet-gevaccineerde personen die besmet waren met de SARS-CoV-2 Delta-variant in een federale gevangenis, juli-augustus 2021. Ze ontdekten dat in totaal 978 exemplaren waren verstrekt door 95 deelnemers, “van wie 78 (82%) waren volledig gevaccineerd en 17 (18%) waren niet volledig gevaccineerd... clinici en volksgezondheidswerkers zouden gevaccineerde personen die besmet raken met SARS-CoV-2 moeten beschouwen als niet minder besmettelijk dan niet-gevaccineerde personen.” |
| 30) Andeweg et al. | Andeweg et al. analyseerde 28,578 gesequenced SARS-CoV-2-monsters van personen met een bekende immuunstatus, verkregen via nationale gemeenschapstesten in Nederland van maart tot augustus 2021. Ze vonden bewijs voor een “verhoogd risico op infectie door de bèta (B.1.351), Gamma ( P.1), of Delta (B.1.617.2) varianten in vergelijking met de Alpha (B.1.1.7) variant na vaccinatie. Er werden geen duidelijke verschillen gevonden tussen vaccins. Het effect was echter groter in de eerste 14-59 dagen na volledige vaccinatie in vergelijking met 60 dagen en langer. In tegenstelling tot door vaccins geïnduceerde immuniteit, werd er geen verhoogd risico op herinfectie met Beta-, Gamma- of Delta-varianten gevonden in vergelijking met de Alpha-variant bij personen met infectie-geïnduceerde immuniteit.” |
| 31) Di Fusco et al. | Di Fusco et al. heeft een evaluatie uitgevoerd van doorbraakinfecties door het COVID-19-vaccin bij immuungecompromitteerde patiënten die volledig zijn gevaccineerd met BNT162b2. “Doorbraakinfecties door het COVID-19-vaccin werden onderzocht bij volledig gevaccineerde (≥14 dagen na de 2e dosis) IC-individuen (IC-cohort), 12 elkaar uitsluitende IC-conditiegroepen en een niet-IC-cohort.” Ze ontdekten dat “van de 1,277,747 personen van ≥16 jaar die 2 doses BNT162b2 kregen, 225,796 (17.7%) werden geïdentificeerd als IC (mediane leeftijd: 58 jaar; 56.3% vrouw). De meest voorkomende IC-aandoeningen waren solide maligniteit (32.0%), nierziekte (19.5%) en reumatologische/inflammatoire aandoeningen (16.7%). Onder de volledig gevaccineerde IC- en niet-IC-cohorten werden tijdens de onderzoeksperiode in totaal 978 doorbraakinfecties waargenomen; 124 (12.7%) resulteerden in ziekenhuisopname en 2 (0.2%) waren intramurale sterfgevallen. IC-individuen waren goed voor 38.2% (N = 374) van alle doorbraakinfecties 59.7% (N = 74) van alle ziekenhuisopnames, en 100% (N = 2) van intramurale sterfgevallen. Het aandeel met doorbraakinfecties was 3 keer hoger in het IC-cohort dan in het niet-IC-cohort (N = 374 [0.18%] vs. N = 604 [0.06%]; ongecorrigeerde incidentiecijfers waren respectievelijk 0.89 en 0.34 per 100 persoonsjaren.” |
| 32) Mallapati (NATUUR) | (NATURE) meldde dat het beschermende effect van vaccinatie als u al een infectie heeft gehad "relatief klein is en alarmerend afneemt drie maanden na ontvangst van de tweede injectie". Mallapaty voegt verder toe wat we de volksgezondheidsgemeenschap hebben gewaarschuwd, namelijk dat personen die besmet zijn met Delta ongeveer dezelfde niveaus van viraal genetisch materiaal in hun neus hebben "ongeacht of ze eerder waren gevaccineerd, wat suggereert dat gevaccineerde en niet-gevaccineerde mensen mogelijk even besmettelijk.” Mallapaty rapporteerde over testgegevens van 139,164 nauwe contacten van 95,716 mensen die tussen januari en augustus 2 in het Verenigd Koninkrijk met SARS-CoV-2021 besmet waren, en op een moment dat de Alpha- en Delta-varianten streden om dominantie. De bevinding was dat “hoewel de vaccins enige bescherming boden tegen infectie en verdere overdracht, Delta dat effect dempte. Een persoon die volledig is ingeënt en vervolgens een 'doorbraak' Delta-infectie had bijna twee keer zoveel kans om het virus door te geven als iemand die besmet was met Alpha. En dat kwam bovenop het grotere risico op een doorbraakinfectie veroorzaakt door Delta dan één veroorzaakt door Alpha.” |
| 33) Chia et al. | Chia et al. rapporteerden dat de waarden van de PCR-cyclusdrempel (Ct) “vergelijkbaar waren tussen zowel gevaccineerde als niet-gevaccineerde groepen bij diagnose, maar dat de virale belasting sneller afnam bij gevaccineerde personen. Vroege, robuuste boosting van anti-spike eiwit-antilichamen werd waargenomen bij gevaccineerde patiënten, maar deze titers waren significant lager tegen B.1.617.2 in vergelijking met de wildtype vaccinstam.” |
| 34) Wilhelm et al. | Wilhelm et al. gerapporteerd over verminderde neutralisatie van SARS-CoV-2 omicron-variant door vaccinsera en monoklonale antilichamen. “in vitro bevindingen met behulp van authentieke SARS-CoV-2-varianten geven aan dat in tegenstelling tot de momenteel circulerende Delta-variant, de neutralisatie-efficiëntie van door vaccins opgewekte sera tegen Omicron ernstig was verminderd, wat de door T-cellen gemedieerde immuniteit benadrukt als essentiële barrière om ernstige COVID-19 te voorkomen. |
| 35) CDC-rapport | CDC rapporteerde over de details van 43 gevallen van COVID-19 toegeschreven aan de Omicron-variant. Ze ontdekten dat “34 (79%) voorkwamen bij personen die de primaire reeks van een door de FDA geautoriseerd of goedgekeurd COVID-19-vaccin ≥14 dagen vóór het begin van de symptomen of ontvangst van een positief SARS-CoV-2-testresultaat voltooiden.” |
| 36) Dejnirattisai et al. | Dejnirattisai et al. presenteerde levende neutralisatietiters tegen de SARS-CoV-2 Omicron-variant en onderzocht deze in verhouding tot neutralisatie tegen de Victoria-, Beta- en Delta-varianten. Ze meldden een significante daling van "neutralisatietiters bij ontvangers van zowel AZD1222- als BNT16b2-basiscursussen, met aanwijzingen dat sommige ontvangers helemaal niet neutraliseerden." |
| 37) Cele et al. | Cele et al. beoordeeld of de Omicron-variant ontsnapt aan antilichaamneutralisatie "veroorzaakt door het Pfizer BNT162b2-mRNA-vaccin bij mensen die alleen zijn gevaccineerd of die zijn gevaccineerd en eerder zijn geïnfecteerd." Ze meldden dat de Omicron-variant "nog steeds de ACE2-receptor nodig had om te infecteren, maar een uitgebreide ontsnapping aan Pfizer veroorzaakte neutralisatie." |
| 38) Holm Hansen et al. | In het Denemarken-onderzoek van Holm Hansen et al. werd gekeken naar de effectiviteit van het vaccin tegen SARS-CoV-2-infectie met de Omicron- of Delta-varianten na een vaccinatiereeks met twee doses of booster BNT162b2 of mRNA-1273. Een belangrijke bevinding werd gerapporteerd als “VE tegen Omicron was aanvankelijk 55.2% na primaire BNT162b2-vaccinatie, maar nam daarna snel af. Hoewel met minder precisie geschat, duidde VE tegen Omicron na primaire mRNA-1273-vaccinatie eveneens op een snelle afname van de bescherming. Ter vergelijking: beide vaccins vertoonden een hogere, langdurigere bescherming tegen Delta.” Met andere woorden, het vaccin dat tegen Delta heeft gefaald, is nog veel erger voor Omicron. Onderstaande tabel en figuur schetsen een vernietigend beeld. Zie waar de groene stip is (Omicron-variant) in de verticale lijnen (blauw is Delta) en de 2 randen van de balken (boven- en onderlip) 91 dagen uit voor Omicron (3 maanden). Zowel Pfizer als Moderna vertonen een negatieve werkzaamheid voor Omicron na 31 dagen (beide bevinden zich onder de 'lijn van geen effect' of '0'). De vergelijkende tabel is zelfs nog verwoestender, omdat hij laat zien hoeveel minder vaccineffectiviteit er is voor Omicron. Na 1-30 dagen toonde Pfizer bijvoorbeeld 55.2% effectiviteit voor Omicron versus 86.7% voor Delta, en voor dezelfde periode toonde Moderna 36.7% effectiviteit voor Omicron versus 88.2% voor Delta. |
| 39) Britse gezondheidsbeveiligingsdienst | Britse rapportage toonde aan dat boosters gedurende ongeveer 19 weken beschermen tegen symptomatische COVID-10 veroorzaakt door Omicron; de Britse gezondheidsbeveiligingsdienst gemelde bescherming tegen symptomatische COVID-19 veroorzaakt door de variant daalde van 70% naar 45% na een Pfizer-booster voor degenen die aanvankelijk waren gevaccineerd met de injectie die door Pfizer met BioNTech is ontwikkeld. Specifiek rapportage door de Britse gezondheidsbeveiligingsdienst toonde aan: “Onder degenen die een primaire AstraZeneca-kuur kregen, was de werkzaamheid van het vaccin ongeveer 60% 2 tot 4 weken na een Pfizer- of Moderna-booster, daarna gedaald tot 35% met een Pfizer-booster en 45% met een Moderna-booster 10 weken na de aanjager. Onder degenen die een primaire Pfizer-kuur kregen, was de werkzaamheid van het vaccin ongeveer 70% na een Pfizer-booster, daalde tot 45% na meer dan 10 weken en bleef ongeveer 70 tot 75% na een Moderna-booster tot 9 weken na de booster.” |
| 40) Buchan et al. | Buchan et al. gebruikte een test-negatief ontwerp om de effectiviteit van het vaccin tegen OMICRON- of DELTA-varianten (ongeacht de symptomen of ernst) te beoordelen op 22 november en 19 december 2021. Onder hen waren personen die ten minste 2 COVID-19-vaccindoses hadden gekregen (met ten minste 1 mRNA-vaccindosis voor de primaire serie) en toegepaste multivariabele logistische regressiemodelleringsanalyse om "de effectiviteit van twee of drie doses te schatten tegen de tijd sinds de laatste dosis." Ze omvatten 3,442 Omicron-positieve gevallen, 9,201 Delta-positieve gevallen en 471,545 test-negatieve controles. Na 2 doses “nam de effectiviteit van het vaccin tegen Delta-infectie in de loop van de tijd gestaag af, maar herstelde zich tot 93% (95% BI, 92-94%) ≥7 dagen na ontvangst van een mRNA-vaccin voor de derde dosis. Daarentegen bood de ontvangst van 2 doses COVID-19-vaccins geen bescherming tegen Omicron. De vaccineffectiviteit tegen Omicron was 37% (95% BI, 19-50%) ≥7 dagen na ontvangst van een mRNA-vaccin voor de derde dosis.” |
| 41) Volksgezondheid Schotland COVID-19 & statistisch winterrapport | Public Health Scotland COVID-19 & Winter Statistical Report (publicatiedatum: 19 januari 2022) leverde verrassende gegevens op pagina 38 (gevallencijfers), pagina 44 (ziekenhuisopname) en pagina 50 (sterfgevallen), waaruit blijkt dat de vaccinatie niet is geslaagd Delta maar kritisch, faalt omicron. De 2nd inentingsgegevens zijn van bijzonder belang. Tabel 14 voor leeftijd gestandaardiseerde casusgegevens is erg verontrustend, omdat het over de meerdere weken van de studie laat zien dat voor elke dosis (1 vs 2 vs 3 boosterinentingen) dat de gevaccineerde veel meer geïnfecteerd zijn dan de niet-gevaccineerde, met de 2nd dosis alarmerend verhoogd is (zie grijze rijen). Naar leeftijd gestandaardiseerde tarieven van acute ziekenhuisopnames zijn verbluffend verhoogd na 2 jaarnd inenting (over de niet-gevaccineerden) in januari 2022. Kijkend naar tabel 16 die het aantal bevestigde COVID-19-gerelateerde sterfgevallen per vaccinatiestatus rapporteert, zien we opnieuw een enorme stijging van het aantal overlijdens op de 2ndinenting. Deze gegevens geven ons aan dat het vaccin geassocieerd is met infectie en niet optimaal werkt tegen omicron en dat de bescherming beperkt is en snel afneemt. |
| 42) Het Britse COVID-19-vaccinbewakingsrapport Week 3, 20 januari 2022 | Het Britse COVID-19-vaccinsurveillancerapport, week 3, 20 januari 2022, geeft aanleiding tot zeer ernstige bezorgdheid over het falen van de vaccins op Delta (dat nu in feite wordt vervangen door omicron voor dominantie) en omicron. Als we kijken naar tabel 9, pagina 34 (COVID-19-gevallen naar vaccinatiestatus tussen week 51 2021 en week 2 2022), zien we grotere aantallen gevallen voor de 2nd en 3rd inentingen. De belangrijke tabel op pagina 38, figuur 12 (niet-gecorrigeerde percentages van COVID-19-infectie, ziekenhuisopname en overlijden bij gevaccineerde en niet-gevaccineerde populaties) toont ons een continu patroon in de Britse gegevens over de afgelopen 2 tot 3 tot 4 maanden, met de huidige rapportage waaruit blijkt dat personen in ontvangst van de 3rd inenting (booster) met een veel groter risico op infectie/gevallen dan niet-gevaccineerden (30 jaar en ouder). |
| 43) Surveillancerapporten voor de Britse volksgezondheid | In de recente UK Public Health surveillance rapporten Week 9, Week 8, evenals week 7 (VK COVID-19 vaccin surveillance rapport Week 7 17 februari 2022), week 6 (COVID-19 vaccin surveillance rapport Week 6 10 februari 2022) en week 5 voor 2022 (COVID-19 vaccin surveillance rapport Week 5 3 februari 2022) evenals de rapporten die zijn verzameld voor 2021 sinds de uitrol van het vaccin, zien we dat de gevaccineerden een hoger risico lopen op infectie en vooral voor leeftijdsgroepen boven de 18 jaar, evenals ziekenhuisopname en zelfs overlijden. Dit geldt met name voor degenen die dubbele vaccinaties krijgen. Er is een verhoogd risico op overlijden voor degenen die drievoudig zijn gevaccineerd en vooral naarmate de leeftijd stijgt. Hetzelfde patroon komt naar voren in de Schotse gegevens. |
| 44.) Regev-Yochay et al. | Regev-Yochay et al. in Israël bekeken (publicatiedatum 16 maartth 2022) de immunogeniciteit en veiligheid van een vierde dosis (4th) van ofwel BNT162b2 (Pfizer-BioNTech) of mRNA-1273 (Moderna) toegediend 4 maanden na de derde dosis in een reeks van drie BNT162b2-doses). Dit was een open-label, niet-gerandomiseerde klinische studie waarin de 4th dosis in termen van behoefte voorbij de 3rd dosis. Van de '1050 in aanmerking komende gezondheidswerkers die deelnamen aan het Sheba HCW COVID-19 Cohort, ontvingen 154 de vierde dosis BNT162b2 en 1 week later ontvingen 120 mRNA-1273. Voor elke deelnemer werden twee op leeftijd afgestemde controles geselecteerd uit de resterende in aanmerking komende deelnemers. Onderzoekers rapporteerden verder dat 'in totaal 25.0% van de deelnemers in de controlegroep geïnfecteerd was met de omicron-variant, vergeleken met 18.3% van de deelnemers in de BNT162b2-groep en 20.7% van die in de mRNA-1273-groep. De werkzaamheid van het vaccin tegen elke SARS-CoV-2-infectie was 30% (95% betrouwbaarheidsinterval [BI], −9 tot 55) voor BNT162b2 en 11% (95% BI, −43 tot 44) voor mRNA-1273... geïnfecteerde deelnemers waren potentieel besmettelijk, met relatief hoge virale ladingen (nucleocapside-gencyclusdrempel, ≤25)'. Resultaten suggereren dat maximale immunogeniciteit van mRNA-vaccins wordt bereikt na drie doses. Meer in het bijzonder stelden onderzoekers een lage vaccineffectiviteit vast tegen infecties bij gezondheidswerkers, evenals relatief hoge virale ladingen die erop wijzen dat degenen die besmet waren besmettelijk waren. Zo kan een vierde vaccinatie van gezonde jonge gezondheidswerkers slechts marginale voordelen opleveren'. |
| 45.) Andries et al. | Andrews et al. gebruikte een test-negatief case-control-ontwerp om de effectiviteit van vaccins tegen symptomatische ziekten veroorzaakt door de varianten omicron en delta (B.1.617.2) in Engeland te schatten. “De effectiviteit van het vaccin werd berekend na primaire immunisatie met twee doses BNT162b2 (Pfizer-BioNTech), ChAdOx1 nCoV-19 (AstraZeneca) of mRNA-1273 (Moderna) vaccin en na een boosterdosis van BNT162b2, ChAdOx1 nCoV-19 of mRNA -1273.” De resultaten toonden aan dat immunisatie met twee doses ChAdOx1 nCoV-19- of BNT162b2-vaccin een zeer beperkte bescherming bood tegen symptomatische ziekte veroorzaakt door de omicron-variant. “Een BNT162b2- of mRNA-1273-booster na de primaire kuur van ChAdOx1 nCoV-19 of BNT162b2 verhoogde de bescherming aanzienlijk, maar die bescherming nam na verloop van tijd af.” |
| 46) Hofmann et al. | Hofmann et al. gepubliceerd in het tijdschrift CELL dat het OMICRON-spike-eiwit (antigeen) neutralisatie door antilichamen van “herstellende patiënten of personen die zijn gevaccineerd met het BioNTech-Pfizer-vaccin (BNT162b2) met een 12- tot 44-voudige hogere efficiëntie dan de spike van de Delta-variant ontwijkt. Neutralisatie van de Omicron-piek door antilichamen die werden geïnduceerd na heterologe ChAdOx1 (Astra Zeneca-Oxford)/BNT162b2-vaccinatie of vaccinatie met drie doses BNT162b2 was efficiënter, maar de Omicron-piek ontweek neutralisatie nog steeds efficiënter dan de Delta-piek.” Over het algemeen toonden de resultaten aan dat de meeste therapeutische antilichamen niet effectief zullen zijn tegen de Omicron-variant en alarmerend genoeg dat dubbele inenting met BNT162b2 (Pfizer) mogelijk niet "voldoende bescherming biedt tegen ernstige ziekten die door deze variant worden veroorzaakt". |
| 47) Baron et al. | Bar-on et al. gepubliceerd in NEJM onder de titel: Bescherming door een vierde dosis BNT162b2 tegen Omicron in Israël. Ze beoordeelden de database van het Israëlische ministerie van Volksgezondheid en verzamelden gegevens over 1,252,331 personen die 60 jaar of ouder waren en in aanmerking kwamen voor de vierde dosis gedurende een periode waarin de B.1.1.529 (omicron) variant van SARS-CoV-2 werd overheersend (10 januari tot 2 maart 2022). De analyse was gericht op het percentage bevestigde infectie en ernstige Covid-19 als functie van de tijd vanaf 8 dagen na ontvangst van een vierde dosis (groepen met vier doses) in vergelijking met die bij personen die slechts drie doses hadden gekregen (drie doses). dosisgroep) en bij personen die 3 tot 7 dagen eerder een vierde dosis hadden gekregen (interne controlegroep). Ze gebruikten een quasi-Poisson-regressiemodellering en met correctie voor confounders, naar verluidt gecorrigeerd voor leeftijd, geslacht, demografische groep en kalenderdag. De belangrijkste bevindingen die het falen van de 4 . onderstrepenth dosis, is als volgt: “Het vergelijken van de snelheidsverhouding in de tijd sinds de vierde dosis (Figuur 2) suggereert dat de bescherming tegen bevestigde infectie met de omicron-variant een maximum bereikt in de vierde week na vaccinatie, waarna de rate ratio in de achtste week daalt tot ongeveer 1.1; deze bevindingen suggereren dat de bescherming tegen bevestigde infectie snel afneemt... Het aangepaste infectiepercentage in de achtste week na de vierde dosis was zeer vergelijkbaar met die in de controlegroepen; de snelheidsverhouding voor de groep met drie doses in vergelijking met de groep met vier doses was 1.1 (95% BI, 1.0 tot 1.2), en de verhouding voor de interne controlegroep in vergelijking met de groep met vier doses was slechts 1.0 ( 95% BI, 0.9 tot 1.1).” Deze bevindingen geven geen verschil aan. We maken ons ook zorgen over de methodologie, aangezien het duidelijk is dat ze niet konden of wilden controleren op dringende verstorende (vervormende) variabelen die de bevindingen zouden kunnen beïnvloeden. Dit kan vaak leiden tot overschatting (of onderschatting) van het behandeleffect. Hebben ze bijvoorbeeld gecontroleerd op eerdere infectie, hebben ze gecontroleerd op drugsgebruik in een vroeg stadium, hebben ze gecorrigeerd voor gedragsverschillen in de 4e dosisgroep, of reeds bestaande aandoeningen, of differentiële behandeling enz. De onderzoekers hielden rekening met enkele vooroordelen, bijv. "Deze mogelijke vooroordelen omvatten de "gezonde gevaccineerde" vooringenomenheid, waarbij mensen die zich ziek voelen de neiging hebben zich de volgende dagen niet te laten vaccineren, wat leidt tot een lager aantal bevestigde infecties en ernstige ziekten in de groep met vier doses gedurende de eerste dagen na vaccinatie. Bovendien zou je verwachten dat detectiebias als gevolg van gedragsveranderingen, zoals de neiging om minder testen te doen na vaccinatie, kort na ontvangst van de dosis meer uitgesproken is.” |
| 48) Duurzaamheid van het BNT162b2-vaccin tegen opnames in ziekenhuizen en spoedeisende hulp vanwege de omicron- en delta-varianten in een groot gezondheidssysteem in de VS: een test-negatieve case-control studie, Tartof, 2022. | Onderzoekers evalueerden de effectiviteit en duurzaamheid van twee en drie doses van het BNT162b2 (Pfizer-BioNTech) mRNA-vaccin tegen opnames in ziekenhuizen en spoedeisende hulp vanwege de delta- (B.1.617.2) en omicron-varianten; een case-control studie met een test-negatief ontwerp, analyseren elektronische gezondheidsdossiers van leden van Kaiser Permanente Southern California (KPSC), een groot geïntegreerd gezondheidssysteem in Californië, VS, van 1 december 2021 tot 6 februari 2022; “Er zijn analyses gedaan voor 11 123 opnames in ziekenhuizen of spoedeisende hulp. In aangepaste analyses was de effectiviteit van twee doses van het BNT162b2-vaccin tegen de omicron-variant 41% (95% BI 21-55) tegen ziekenhuisopname en 31% (16-43) tegen opname op de spoedeisende hulp 9 maanden of langer na de tweede dosis"; onderzoekers meldden ook dat "3 maanden na ontvangst van een derde dosis, afname duidelijk was tegen SARS-CoV-2-resultaten vanwege de omicron-variant, inclusief ziekenhuisopname." |
| 49) Laith J. Abu-Raddad et al. (mei 2022): | “Effect van mRNA-vaccinboosters tegen SARS-CoV-2 Omicron-infectie in Qatar”; zoals we zien, het vaccin heeft gefaald, VE is <50% (de benodigde drempel) en '0' sterfgevallen; “Twee gematchte retrospectieve cohortstudies om de effectiviteit van boostervaccinatie te beoordelen, vergeleken met die van alleen een primaire serie met twee doses, tegen symptomatische SARS-CoV-2-infectie en Covid-19-gerelateerde ziekenhuisopname en overlijden tijdens een grote golf van omicron infecties van 19 december 2021 tot en met 26 januari 2022. De associatie van boosterstatus met infectie werd geschat met behulp van Cox-regressiemodellen voor proportionele risico's. Zoals we zien, heeft het vaccin gefaald, VE is <50% (de benodigde drempel) en '0' sterfgevallen. De belangrijkste bevindingen zijn als volgt om aan te tonen dat de vaccins de drempel van 50% voor effectiviteit niet halen: Effectiviteit van BNT162b2 Booster tegen Omicron-variant "De geschatte effectiviteit van de BNT162b2-booster (Pfizer) tegen symptomatische omicron-infectie, vergeleken met die van de primaire serie met twee doses, was 49.4% (95% BI, 47.1 tot 51.6)." Effectiviteit van mRNA-1273 Booster tegen Omicron-variant "De geschatte effectiviteit van de mRNA-1273-booster (Moderna), vergeleken met die van de primaire serie met twee doses, was 47.3% (95% BI, 40.7 tot 53.3)." Aanvullende analyses “Voor de BNT162b2-vaccinanalyse, met de start van de follow-up op de 15e dag na de boostervaccinatie, was de geschatte effectiviteit van de booster tegen symptomatische omicron-infectie, in vergelijking met die van de primaire serie met twee doses, 49.9% ( 95% BI, 47.6 tot 52.2) (Fig. S2 en Tabel S4). De overeenkomstige geschatte werkzaamheid van het mRNA-1273-vaccin was 52.0% (95% BI, 45.1 tot 57.9). Beide schattingen van de effectiviteit waren vergelijkbaar met die in de hoofdanalyse. De geschatte werkzaamheid van de BNT162b2-vaccinbooster tegen symptomatische omicron-infectie, vergeleken met die van de primaire serie met twee doses, was 38.0% (95%-BI, 28.8 tot 46.0) bij personen die de booster 8 maanden of minder na de tweede dosis en 50.5% (95% BI, 48.2 tot 52.8) bij degenen die het meer dan 8 maanden na de tweede dosis kregen. De overeenkomstige schattingen van de effectiviteit van het mRNA-1273-vaccin waren 41.5% (95% BI, 32.3 tot 49.5) en 56.8% (95% BI, 47.0 tot 64.8).” |
| 50) Fleming-Dutra et al. | Fleming-Dutra et al. onderzocht de associatie van eerdere BNT162b2 COVID-19-vaccinatie met symptomatische SARS-CoV-2-infectie bij kinderen en adolescenten tijdens overheersing van Omicron. Zij gebruikten een test-negatieve, case-control studie uitgevoerd van december 2021 tot februari 2022 tijdens de overheersing van de Omicron-variant met 121 952 tests van locaties in de VS, de geschatte werkzaamheid van het vaccin tegen symptomatische infectie voor kinderen van 5 tot 11 jaar was 60.1% 2 tot 4 weken na dosis 2 en 28.9% tijdens maand 2 na dosis 2. Bij adolescenten van 12 tot 15 jaar was de geschatte werkzaamheid van het vaccin 59.5% 2 tot 4 weken na dosis 2 en 16.6% tijdens maand 2 (zie figuur 2). Zij concludeerden dat "bij kinderen en adolescenten de geschatte werkzaamheid van het vaccin voor 2 doses BNT162b2 tegen symptomatische infectie snel afnam". We zien VE dalen tot onder 0 na ongeveer 4.5 maanden. |
| 51) Lassauniere et al: | Lassauniere et al: “Neutraliseren van antilichamen tegen de SARS-CoV-2 Omicron-variant (BA.1) 1 tot 18 weken na de tweede en derde dosis van het BNT162b2 mRNA-vaccin”; “Ons onderzoek vond een snelle afname van Omicron-specifieke serumneutraliserende antilichaamtiters slechts een paar weken na de tweede en derde dosis BNT162b2….de waargenomen afname van populatieneutraliserende antilichaamtiters komt overeen met de afname van de werkzaamheid van het vaccin tegen polymerasekettingreactie – bevestigd Omicron-infectie in Denemarken en symptomatische Omicron-infectie in het Verenigd Koninkrijk… Alles bij elkaar genomen zijn door vaccins geïnduceerde beschermende antilichaamresponsen na een tweede en derde dosis BNT162b2 van voorbijgaande aard en aanvullende boosterdoses kunnen nodig zijn, vooral bij oudere mensen; geconserveerde T-celimmuniteit en niet-neutraliserende antilichamen kunnen echter nog steeds bescherming bieden tegen ziekenhuisopname en overlijden." |
| 52) Bescherming en afname van natuurlijke en hybride immuniteit voor SARS-CoV-2 | “Het aantal gevallen van SARS-CoV-2-infectie per 100,000 persoonsdagen met risico (gecorrigeerd percentage) nam toe met de tijd die was verstreken sinds vaccinatie met BNT162b2 of sinds eerdere infectie. Onder niet-gevaccineerde personen die hersteld waren van infectie, steeg dit percentage van 10.5 onder degenen die 4 tot minder dan 6 maanden eerder waren geïnfecteerd tot 30.2 onder degenen die 1 jaar of langer eerder waren geïnfecteerd. Bij personen die na een eerdere infectie een enkele dosis vaccin hadden gekregen, was het aangepaste percentage laag (3.7) bij degenen die minder dan 2 maanden eerder waren gevaccineerd, maar steeg het tot 11.6 bij degenen die minstens 6 maanden eerder waren gevaccineerd. Onder voorheen niet-geïnfecteerde personen die twee doses vaccin hadden gekregen, steeg het aangepaste percentage van 21.1 onder degenen die minder dan 2 maanden eerder waren gevaccineerd tot 88.9 onder degenen die ten minste 6 maanden eerder waren gevaccineerd. Onder personen die eerder met SARS-CoV-2 waren geïnfecteerd (ongeacht of ze een dosis vaccin hadden gekregen of één dosis voor of na infectie hadden gekregen), nam de bescherming tegen herinfectie af naarmate de tijd sinds de laatste immuniteit toenam. verlenende gebeurtenis; deze bescherming was echter hoger dan die welke werd verleend nadat dezelfde tijd was verstreken sinds de ontvangst van een tweede dosis vaccin bij voorheen niet-geïnfecteerde personen. Een enkele dosis vaccin na infectie versterkte de bescherming tegen herinfectie.” |
| 53) CDC en afnemende 2-dosis en 3-dosis effectiviteit van mRNA-vaccins tegen COVID-19-geassocieerde afdeling spoedeisende hulp en spoedeisende zorg en ziekenhuisopnames bij volwassenen tijdens perioden van overheersing van delta- en Omicron-varianten - VISION Network, 10 staten, augustus 2021 - januari 2022 , Ferdinands, 2022: | “Tijdens de Omicron-overheersende periode was VE tegen COVID-19-geassocieerde ED/UC-ontmoetingen over het algemeen lager in vergelijking met die tijdens de Delta-overheersende periode en nam af na de tweede dosis, van 69% binnen 2 maanden na vaccinatie tot 37% bij ≥5 maanden na vaccinatie (p<0.001). De bescherming nam toe na een derde dosis, met een VE van 87% onder degenen die in de afgelopen 2 maanden waren gevaccineerd; VE nam na 3 doses echter af tot 66% bij degenen die 4-5 maanden eerder waren gevaccineerd en 31% bij degenen die ≥5 maanden eerder waren gevaccineerd”...in een multistate-analyse van 241,204 ED/UC-ontmoetingen en 93,408 ziekenhuisopnames bij volwassenen met COVID-19– zoals ziekte tussen 26 augustus 2021 en 22 januari 2022, waren schattingen van VE tegen door laboratoriumonderzoek bevestigde COVID-19 lager tijdens de Omicron-overheersende periode dan tijdens de Delta-overheersende periode, rekening houdend met zowel het aantal ontvangen vaccindoses als de tijd sindsdien vaccinatie. Tijdens beide perioden was de VE na ontvangst van een derde dosis altijd hoger dan de VE na een tweede dosis; VE nam echter af met toenemende tijd sinds vaccinatie. |
| 54) Ernstige COVID-19-resultaten na volledige vaccinatie van het primaire schema en initiële boosters: gepoolde analyse van nationale prospectieve cohortstudies van 30 miljoen personen in Engeland, Noord-Ierland, Schotland en Wales, Agrawal et al., oktober 2022 | “Er was een verhoogd risico op ernstige COVID-19-uitkomsten 10 weken na het voltooien van de primaire doses BNT162b2 of ChAdOx1 nCoV-19 (≥20 weken vs 3-9 weken; aRR 4 [55% BI 95-4]). Personen met een groter aantal comorbiditeiten (≥16 comorbiditeiten vs geen; 7·98 [7·73–8·24], die ouder waren (in de leeftijd van ≥80 jaar .) vs 18-49 jaar; 8·12 [7·89–8·35]), die een hogere BMI hadden (≥40 vs 18–5; 24 [9·1–75]), of die man waren (mannelijk vs vrouw; 1·19 [1·17–1·21]) werden ook in verband gebracht met een verhoogd risico op ernstige COVID-19-uitkomsten.” Dit bevolkingsonderzoek in het hele VK van meer dan 16 miljoen in Engeland, Noord-Ierland, Schotland en Wales heeft geconstateerd dat, na de eerste boostervaccinatie, ouderen, mensen met een hoge multimorbiditeit en mensen met bepaalde onderliggende gezondheidsproblemen het grootste risico lopen op COVID-19-gerelateerde ziekenhuisopname en overlijden. Deze bevindingen zijn zeer problematisch voor de voorstanders van vaccins. Het COVID-geninjectievaccin heeft gefaald, is niet-steriliserend, niet-neutraliserend, beschermt de bovenste luchtwegen niet (voorkomt geen infectie of overdracht) en beschermt de onderste longen niet effectief of behoorlijk tegen ernstige ziekten. |
| 55) Afnemende eerste en tweede dosis ChAdOx1- en BNT162b2 COVID-19-vaccinaties: een gepoolde proefstudie met 12.9 miljoen personen in Engeland, Noord-Ierland, Schotland en Wales, Kerr, 2022 | “Voor Doses 1 en 2 van ChAdOx1 en Dosis 1 van BNT162b2, bereikte VE/rVE nul op ongeveer 60-80 dagen en werd toen negatief. Op dag 70 was VE/rVE -25% (95% BI: -80 tot 14) en 10% (95% BI: -32 tot 39) voor respectievelijk Doses 1 en 2 van ChAdOx1, en 42% (95% BI: -9 tot 64) BI: 53 tot 95) en 26% (70% BI: 1 tot 2) voor respectievelijk Doses 162 en 2 van BNT2b162. De rVE voor dosis 2 van BNT46b95 bleef de hele tijd boven nul en bereikte 13% (67%-BI: 98 tot XNUMX) na XNUMX dagen follow-up. Sterk bewijs gevonden van afnemende VE/rVE voor Doses 1 en 2 van ChAdOx1, evenals Dosis 1 van BNT162b2.” Deze bevindingen zijn niet onbekend bij de volksgezondheidsinstanties. In werkelijkheid, CDC-directeur Rochelle Walensky heeft gezegd dat de Covid-vaccins “uitzonderlijk goed” werken tegen ernstige ziekte en overlijden, maar “wat ze niet meer kunnen doen, is overdracht voorkomen.” Wat deze onderzoeken laten zien, is dat vaccins belangrijk zijn om ernstige ziekten en sterfte te verminderen, maar niet in staat zijn te voorkomen dat de ziekte zich verspreidt en uiteindelijk de meesten van ons infecteert. Dat wil zeggen, terwijl de vaccins individuele voordelen bieden aan de gevaccineerde, en vooral aan oudere risicovolle mensen, is het publieke voordeel van universele vaccinatie in ernstige twijfel. Als zodanig mag niet worden verwacht dat Covid-vaccins bijdragen aan het elimineren van de gemeenschappelijke verspreiding van het virus of het bereiken van groepsimmuniteit. Dit ontrafelt de grondgedachte voor vaccinmandaten en paspoorten. |
| 56.) Follow-up van zes maanden na een vierde BNT162b2-vaccinatiedosis, Canetti & Regev-Yochay, 2022 | “Van de deelnemers die geen eerdere SARS-CoV-2-infectie hadden gehad, werden er 6113 opgenomen in de analyse van de humorale respons en 11,176 in de analyse van de effectiviteit van het vaccin (Fig. S1 en Tabellen S2 en S3). De antilichaamrespons piekte na ongeveer 4 weken, nam na 13 weken af tot niveaus die vóór de vierde dosis werden waargenomen en stabiliseerde daarna. Gedurende de follow-upperiode van 6 maanden waren de aangepaste wekelijkse niveaus van IgG en neutraliserende antilichamen vergelijkbaar na ontvangst van de derde en vierde dosis en waren aanzienlijk hoger dan de niveaus die werden waargenomen na ontvangst van de tweede dosis (Figuur 1A en 1B en Tabel S4). De cumulatieve incidentiecurve wordt weergegeven in figuur S2 en de effectiviteit van het vaccin wordt weergegeven in Figuur 1C. De ontvangst van de vierde dosis BNT162b2-vaccin bood meer bescherming tegen SARS-CoV-2-infectie dan de ontvangst van drie vaccindoses (waarbij de ontvangst van de derde dosis minstens 4 maanden eerder plaatsvond) (algemene vaccineffectiviteit, 41%; 95% betrouwbaarheidsinterval [BI], 35 tot 47). Tijdspecifieke vaccineffectiviteit (die in onze analyse de infectiepercentages vergeleek onder deelnemers die sinds de vaccinatie nog niet waren geïnfecteerd) nam met de tijd af en nam af van 52% (95% BI, 45 tot 58) gedurende de eerste 5 weken na vaccinatie tot -2% (95% BI, -27 tot 17) na 15 tot 26 weken." 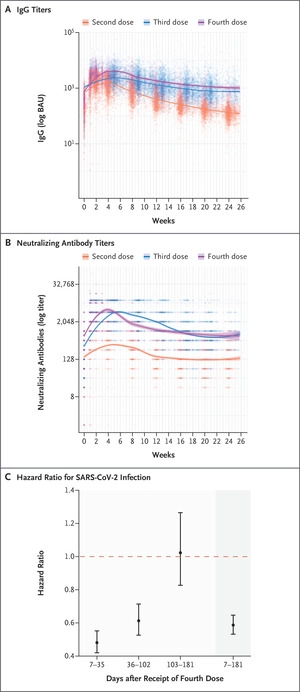 |
| 57) Effectiviteit van mRNA-1273 tegen SARS-CoV-2 omicron- en deltavarianten, Tseng, 2022 | “De 2-dosis VE tegen omicron-infectie na 14-90 dagen was 44.0% (95% BI, 35.1-51.6%), maar daalde snel. De VE met 3 doses was 93.7% (92.2–94.9%) en 86.0% (78.1–91.1%) tegen delta-infectie en 71.6% (69.7–73.4%) en 47.4% (40.5–53.5%) tegen omicroninfectie op 14- respectievelijk 60 dagen en >60 dagen. De VE van 3 doses was 29.4% (0.3-50.0%) tegen omicron-infectie bij immuungecompromitteerde individuen. De 3-dosis VE tegen ziekenhuisopname met delta of omicron was >99%. Onze bevindingen tonen een hoge, duurzame VE van 3 doses tegen delta-infectie, maar een lagere effectiviteit tegen omicron-infectie, vooral bij immuungecompromitteerde mensen. 3-dosis VE was echter hoog tegen ziekenhuisopname met delta of omicron.” |
| 58) Percentage SARS-CoV-2-herinfectie tijdens een Omicron-golf in IJsland, Eythorsson, 2022 | “11 536 PCR-positieve personen werden opgenomen. De gemiddelde (SD) leeftijd was 34 (19) jaar (mediaan 31 jaar; bereik 0-102 jaar), 5888 (51%) waren mannen, 2942 (25.5%) hadden ten minste 1 dosis vaccin gekregen en de gemiddelde (SD) tijd vanaf de eerste infectie was 287 (191) dagen (mediaan, 227 dagen; bereik, 60-642 dagen); De kans op herinfectie nam toe met de tijd vanaf de eerste infectie (odds ratio van 18 maanden versus 3 maanden, 1.56; 95% BI, 1.18-2.08) (Figuur) en was hoger bij personen die 2 of meer doses hadden gekregen in vergelijking met 1 dosis of minder vaccin (odds ratio, 1.42; 95% BI, 1.13-1.78)” |
| 59) Effectiviteit van mRNA-1273 tegen infectie en COVID-19-ziekenhuisopname met SARSCoV-2 Omicron-subvarianten: BA.1, BA.2, BA.2.12.1, BA.4 en BA.5, Tseng, 2022 | “Terwijl 3-dosis VE tegen BA.1-infectie hoog was en langzaam afnam, was VE tegen BA.2, BA.2.12.1, BA.4 en BA.5-infectie aanvankelijk matig tot hoog (61.0%-90.6% 14 -30 dagen na de derde dosis) en nam snel af. De VE van 4 doses tegen infectie met BA.2, BA.2.12.1 en BA.4 varieerde tussen 64.3%-75.7%, en was laag (30.8%) tegen BA.5 14-30 dagen na de vierde dosis en verdween langer dan 90 dagen voor alle subvarianten.” |
| 60) Effectiviteit van COVID-19-vaccins gedurende 13 maanden gedurende de periode van de opkomst van de Omicron-variant in de Zweedse bevolking, Yu, 2022 | “Twee vaccindoses toonden langdurige goede bescherming tegen infectie vóór Omicron (VE was boven de 85% voor alle tijdsintervallen), maar minder bescherming tegen Omicron-infectie (gedaald tot 43% in week vier en geen bescherming in week 14). Evenzo was VE tegen ziekenhuisopname hoog en stabiel vóór Omicron, maar vertoonde een duidelijke afname tijdens de Omicron-periode, hoewel VE-schattingen aanzienlijk hoger waren (meer dan 80% tot week 25, dalend tot 40% in week 40) dan tegen infectie. |
| 61) Langdurige COVID-19-boostereffectiviteit door infectiegeschiedenis en klinische kwetsbaarheid en imprinting van het immuunsysteem, Chematelly, 2022 | “De effectiviteit van de booster ten opzichte van de primaire serie was 41.1% (95% BI: 40.0-42.1%) tegen infectie en 80.5% (95% BI: 55.7-91.4%) tegen ernstige, kritieke of dodelijke COVID-19, gedurende een jaar opvolging na de booster. Onder personen die klinisch kwetsbaar waren voor ernstige COVID-19, was de effectiviteit 49.7% (95% BI: 47.8-51.6%) tegen infectie en 84.2% (95% BI: 58.8-93.9%) tegen ernstige, kritieke of fatale COVID-19. De effectiviteit tegen infectie was het hoogst met 57.1% (95% BI: 55.9-58.3%) in de eerste maand na de booster, maar nam daarna af en was bescheiden met slechts 14.4% (95% BI: 7.3-20.9%) tegen de zesde maand. In de zevende maand en daarna, samenvallend met BA.4/BA.5 en BA.2.75* subvariante incidentie, was de effectiviteit progressief negatief en bereikte -20.3% (95% BI: -55.0-29.0%) na één jaar follow-up . Vergelijkbare beschermingsniveaus en -patronen werden waargenomen ongeacht eerdere infectiestatus, klinische kwetsbaarheid of type vaccin (BNT162b2 versus mRNA-1273).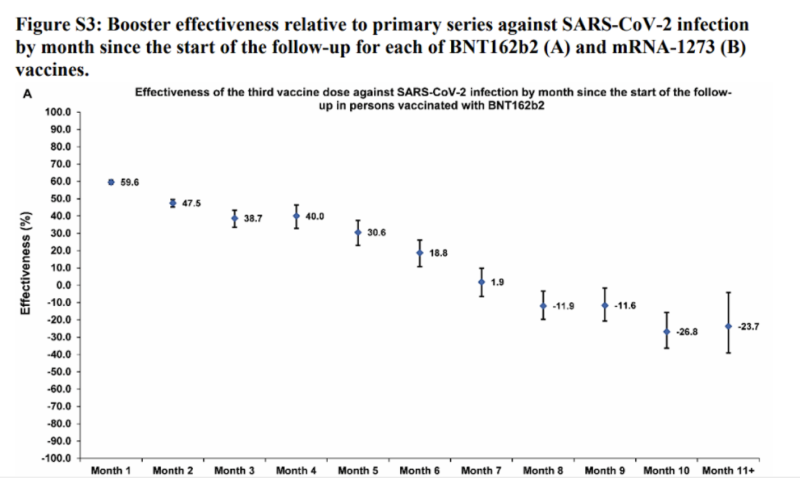 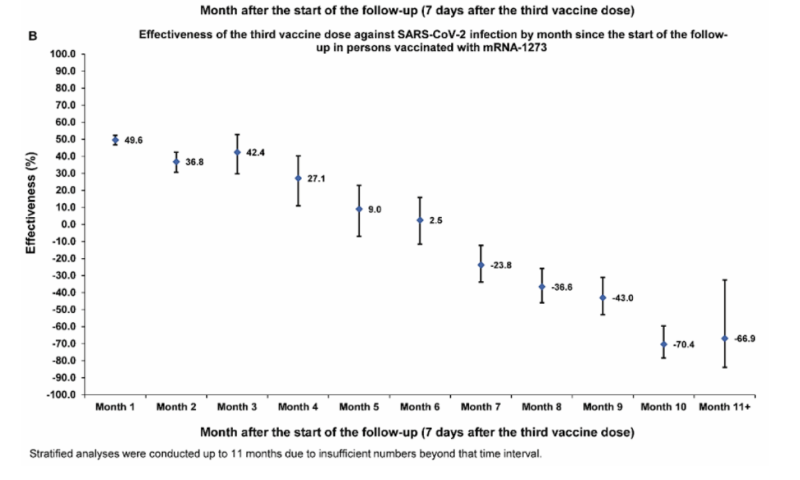 |
| 62) Alarmerende antilichaamontwijkingseigenschappen van stijgende SARS-CoV-2 BQ- en XBB-subvarianten, Wang, 2022 | “BQ.1, BQ.1.1, XBB en XBB.1 zijn tot nu toe de meest resistente SARS-CoV-2-varianten; Serumneutralisatie was duidelijk verminderd, ook met de bivalente booster; Alle klinische monoklonale antilichamen werden inactief gemaakt tegen deze varianten; De ACE2-affiniteit van deze varianten was vergelijkbaar met die van hun ouderstammen; De BQ- en XBB-subvarianten van SARS-CoV-2 Omicron breiden zich nu snel uit, mogelijk als gevolg van gewijzigde antilichaamontduikingseigenschappen die voortkomen uit hun extra spike-mutaties. Hier rapporteren we dat de neutralisatie van BQ.1, BQ.1.1, XBB en XBB.1 door sera van gevaccineerden en geïnfecteerde personen aanzienlijk was aangetast, inclusief sera van personen die een boost hadden gekregen met een WA1/BA.5 bivalent mRNA-vaccin. Titers tegen BQ- en XBB-subvarianten waren respectievelijk 13-81-voudig en 66-155-voudig lager, ver boven wat tot nu toe was waargenomen. Monoklonale antilichamen die de oorspronkelijke Omicron-variant konden neutraliseren, waren grotendeels inactief tegen deze nieuwe subvarianten en de verantwoordelijke individuele spike-mutaties werden geïdentificeerd. Deze subvarianten bleken vergelijkbare ACE2-bindende affiniteiten te hebben als hun voorgangers. Samen geven onze bevindingen aan dat BQ- en XBB-subvarianten een ernstige bedreiging vormen voor de huidige COVID-19-vaccins, alle geautoriseerde antilichamen inactief maken en mogelijk een dominantie hebben verworven in de bevolking vanwege hun voordeel in het ontwijken van antilichamen. |
| 63) Lage neutralisatie van SARS-CoV-2 Omicron BA.2.75.2, BQ.1.1 en XBB.1 door ouderlijk mRNA-vaccin of een BA.5-bivalente booster, Kurhade, 2022 | “De nieuw opgekomen SARS-CoV-2 Omicron-sublijnen, waaronder de BA.2-afgeleide BA.2.75.2 en de BA.5-afgeleide BQ.1.1 en XBB.1, hebben extra spike-mutaties verzameld die de effectiviteit van het vaccin kunnen beïnvloeden. Hier rapporteren we neutraliserende activiteiten van drie menselijke serumpanels verzameld van personen 23-94 dagen na dosis 4 van een ouderlijk mRNA-vaccin, 14-32 dagen na een BA.5-bivalent-booster van personen met 2-4 eerdere doses ouderlijk mRNA vaccin, of 15–32 dagen na een BA.5-bivalente booster van personen met een eerdere SARS-CoV-2-infectie en 2–4 doses ouderlijk mRNA-vaccin. De resultaten toonden aan dat een BA.5-bivalente booster een hoge neutraliserende titer opwekte tegen BA.4/5, gemeten 14 tot 32 dagen na de booster; de BA.5-bivalente booster produceerde echter geen robuuste neutralisatie tegen de nieuw opgekomen BA.2.75.2, BQ.1.1 of XBB.1. Eerdere infectie heeft de omvang en breedte van BA.5-bivalente-booster-opgewekte neutralisatie aanzienlijk verbeterd. Onze gegevens ondersteunen een strategie voor het bijwerken van vaccins waarbij toekomstige boosters moeten passen bij nieuw opgekomen circulerende SARS-CoV-2-varianten.” |
| 64) Effectiviteit van het bivalent vaccin tegen de ziekte van Coronavirus 2019 (COVID-19)., Shrestha, 2022 | “Een retrospectieve cohortstudie uitgevoerd bij het Cleveland Clinic Health System (CCHS) in de Verenigde Staten. Onderzoekers includeerden werknemers op de dag dat het bivalente COVID-19-vaccin voor het eerst beschikbaar was. 'Bescherming door vaccinatie (geanalyseerd als een tijdsafhankelijke covariabele) werd geëvalueerd met behulp van Cox proportionele gevarenregressie.' De bevindingen waren gericht op 51,011 werknemers, waarvan 20,689 (41%) een eerdere gedocumenteerde COVID-19-infectie (episode) hadden, en waarbij 42,064 (83%) ten minste twee doses van het vaccin kregen. 'De meerderheid van de infecties in Ohio werd veroorzaakt door de BA.4- of BA.5-lijnen van de Omicron-variant tijdens de eerste 10 weken van het onderzoek, gebaseerd op monitoringgegevens van de SARS-CoV-2-variant die beschikbaar zijn van het Ohio Department of Health. In december waren de lijnen BQ.1, BQ.1.1 en BF.7 verantwoordelijk voor een aanzienlijk deel van de infecties.' 'Tegen het einde van de studie waren 10804 (21%) geboost met een bivalent vaccin. Het bivalente vaccin was het Pfizer-vaccin in 9595 (89%) en het Moderna-vaccin in de resterende 1178. In totaal kregen 2452 werknemers (5%) COVID-19 tijdens de 13 weken van het onderzoek.' 'De berekende totale vaccineffectiviteit van het model was 30% (95% BI, 20% – 39%)...toen de Omicron BA.4/BA.5-stammen de overheersende circulerende stammen waren.' 'Uit de multivariabele analyses bleek ook dat hoe recenter de laatste eerdere COVID-19-episode was, hoe lager het risico op COVID-19 was, en dat hoe groter het aantal eerder ontvangen vaccindoses, hoe hoger het risico op COVID-19.' |
| 65) Effectiviteit van tweede booster in vergelijking met eerste booster en bescherming verleend door eerdere SARS CoV-2-infectie tegen symptomatische Omicron BA.2 en BA.4/5 in Frankrijk, Tamandjou, 2023 | “We includeerden symptomatische ≥60 jaar oude personen die werden getest op SARSCoV-2 van 21 maart tot 30 oktober 2022. Vergeleken met een eerste booster van 181-210 dagen oud herstelde een tweede booster de bescherming met een effectiviteit van 39% [95%CI: 38% – 41%], 7-30 dagen na vaccinatie Deze winst in bescherming was lager dan die waargenomen met de eerste booster, op gelijke tijdstippen sinds vaccinatie.” |
| 66) Verlengde SARS-CoV-2 RBD-boostervaccinatie induceert humorale en cellulaire immuuntolerantie bij muizen, Gao, 2023 | i) Onze bevindingen tonen potentiële risico's aan bij het continue gebruik van SARS-CoV-2-vaccinversterkers, wat onmiddellijke implicaties heeft voor de wereldwijde COVID-19-vaccinatieverbeteringsstrategieën. ii) Of een dergelijk herstel van de door vaccins geïnduceerde immuunrespons kan worden herhaald door voortgezette toepassing van boosters, wordt in twijfel getrokken, maar is op dit moment grotendeels onbekend. Hier vergeleken we de effecten van herhaalde RBD-vaccinboosters met een conventionele immunisatiekuur met die met een uitgebreide vaccinatiestrategie, in een Balb/c-muismodel. iii) We ontdekten dat de beschermende effecten van de humorale immuniteit en de cellulaire immuniteit die door de conventionele immunisatie tot stand werden gebracht, beide ernstig werden aangetast tijdens de verlengde vaccinatiekuur. Met name verlengde vaccinatie verminderde niet alleen de hoeveelheid en de neutraliserende werkzaamheid van serum-RBD-specifieke antilichamen volledig, maar verkortte ook het humorale geheugen op lange termijn. iv) Dit wordt geassocieerd met immuuntolerantie in de reactie van het kiemcentrum, samen met een verminderd aantal B- en Tfh-cellen in het kiemcentrum van de milt. Bovendien hebben we aangetoond dat verlengde immunisatie de functionele reacties van CD4+- en CD8+T-cellen verminderde, de populatie geheugen-T-cellen inperkte en de expressie van PD-1 en LAG-3 in Te-subtypecellen verhoogde. v) Er werd ook een verhoogd percentiel van Treg-cellen waargenomen, vergezeld van een significante verhoging van de IL-10-productie. Samen hebben we cruciaal bewijs geleverd dat herhaalde toediening van RBD-boostervaccins een negatieve invloed kan hebben op de immuunrespons die tot stand komt door een conventionele vaccinatiekuur en adaptieve immuuntolerantie kan bevorderen.' vi) Voortgezette vaccinatie bevorderde de vorming van een prominente adaptieve immuuntolerantie en verslechterde de gevestigde immuunrespons met de conventionele cursus ernstig, wat blijkt uit significante verminderingen van antigeenspecifieke antilichamen en T-celrespons, een verlies van immuungeheugen en een vorm van immunosuppressieve micro-omgeving . |
| 67) Effect van eerdere infectie, vaccinatie en hybride immuniteit tegen symptomatische BA.1 en BA.2 Omicron-infecties en ernstige COVID-19 in Qatar, Altarawneh, maart 2022 | “Qatar-onderzoekers onderzochten SARS-CoV-2 Omicron symptomatische BA.1-infectie, symptomatische BA.2-infectie, BA.1 ziekenhuisopname en overlijden, en BA.2 ziekenhuisopname en overlijden, tussen 23 december 2021 en 21 februari 2022. De onderzoekers er werden 6 nationale, gematchte, test-negatieve case-control studies uitgevoerd om de effectiviteit van het BNT162b2 (Pfizer-BioNTech) vaccin, het mRNA-1273 (Moderna) vaccin, natuurlijke immuniteit als gevolg van eerdere infectie met pre-Omicron-varianten en hybride immuniteit te onderzoeken van eerdere infectie en vaccinatie. Ze ontdekten dat “de effectiviteit van alleen eerdere infectie tegen symptomatische BA.2-infectie 46.1% was (95% BI: 39.5-51.9%). De effectiviteit van slechts twee doses BNT162b2-vaccinatie was verwaarloosbaar met -1.1% (95%-BI: -7.1-4.6), maar bijna alle personen hadden hun tweede dosis enkele maanden eerder gekregen. De effectiviteit van slechts drie doses BNT162b2-vaccinatie was 52.2% (95% BI: 48.1-55.9%). Effectiviteit van hybride immuniteit van eerdere infectie en vaccinatie met twee doses BNT162b2 was 55.1% (95% BI: 50.9-58.9%).” De belangrijkste bevinding was: "Er zijn geen waarneembare verschillen in de effecten van eerdere infectie, vaccinatie en hybride immuniteit tegen BA.1 versus BA.2." |
| 68) Effectiviteit van een vierde dosis mRNA COVID-19-vaccin tegen sterfte door alle oorzaken bij bewoners van instellingen voor langdurige zorg en bij de oudste ouderen: een landelijke, retrospectieve cohortstudie in Zweden, Nordstrom, 2022 | “Vanaf 7 dagen na baseline waren er 1119 sterfgevallen in het LTCF-cohort tijdens een mediane follow-up van 77 dagen en een maximale follow-up van 126 dagen. Gedurende dag 7 tot 60 was de VE van de vierde dosis 39% (95% BI, 29-48), die daalde tot 27% (95% BI, -2-48) gedurende dag 61 tot 126. In het cohort van alle personen van ≥80 jaar waren er 5753 sterfgevallen tijdens een mediane follow-up van 73 dagen en een maximale follow-up van 143 dagen. Tijdens dagen 7 tot 60 was de VE van de vierde dosis 71% (95% BI, 69-72), die daalde tot 54% (95% BI, 48-60) gedurende dagen 61 tot 143.” |
| 69) Risico op infectie, ziekenhuisopname en overlijden tot 9 maanden na een tweede dosis COVID-19-vaccin: een retrospectieve, totale populatiecohortstudie in Zweden, Nordstrom, 2022 | "Voor de uitkomst SARS-CoV-2-infectie, ongeacht de ernst, nam de vaccineffectiviteit van BNT162b2 geleidelijk af in de loop van de tijd, van 92% (95% BI 92 tot 93; p<0) na 001-15 dagen tot 30% ( 47 tot 39; p<55) na 0-001 dagen, en tot 121% (-180 tot 23; p=2) vanaf dag 41. Het afnemen was iets langzamer voor mRNA-0, met een vaccineffectiviteit van 07% (211 tot 1273; p<96) na 94-97 dagen en 0% (001 tot 15; p=30) vanaf dag 59 . Het afnemen was ook iets langzamer voor heterologe ChAdOx18 nCoV-79 plus een mRNA-vaccin, waarvoor de vaccineffectiviteit 0% (012 tot 181; p<1) was na 19-89 dagen en 79% (94 tot 0; p<001 ·15) vanaf dag 30. Daarentegen was de vaccineffectiviteit voor het homologe ChAdOx66 nCoV-41-vaccin 80% (0 tot 001; p<121) na 1-19 dagen, met geen detecteerbare effectiviteit vanaf dag 68 (-52% [-79 tot 0] ;p=001·15). Voor de uitkomst van ernstige COVID-30 nam de effectiviteit van het vaccin af van 121% (19 tot 98; p<28) na 0-49 dagen tot 19% (89 tot 82; p<93) vanaf dag 0. Over het algemeen was er enig bewijs voor een lagere vaccineffectiviteit bij mannen dan bij vrouwen en bij oudere personen dan bij jongere personen.” |
| 70) Neutralisatie tegen BA.2.75.2, BQ.1.1 en XBB van mRNA Bivalent Booster, Davis Gardner, 2023 | "Gebruikte de FRNT in een VeroE6/TMPRSS2 cellijn1 om de neutraliserende activiteit te vergelijken in serummonsters verkregen van deelnemers in drie cohorten: het eerste cohort bestond uit 12 deelnemers 7 tot 28 dagen na één monovalente booster; de tweede, 11 deelnemers 6 tot 57 dagen na een tweede monovalente booster; en de derde, 12 deelnemers 16 tot 42 dagen na een bivalente booster. In alle drie de cohorten was de neutralisatieactiviteit lager tegen alle omicron-subvarianten dan tegen de WA1/2020-stam; neutraliserende activiteit was het laagst tegen de XBB-subvariant (Figuur 1 en afb. S2). In het cohort dat één monovalente booster ontving, de FRNT50 GMT's waren 857 tegen WA1/2020, 60 tegen BA.1, 50 tegen BA.5, 23 tegen BA.2.75.2, 19 tegen BQ.1.1 en onder de detectielimiet tegen XBB. In het cohort dat twee monovalente boosters ontving, de FRNT50 GMT's waren 2352 tegen WA1/2020, 408 tegen BA.1, 250 tegen BA.5, 98 tegen BA.2.75.2, 73 tegen BQ.1.1 en 37 tegen XBB. De resultaten in beide cohorten komen overeen met neutralisatietiters tegen BA.1 en BA.5 die 5 tot 9 keer zo laag waren als die tegen WA1/2020 en neutralisatietiters tegen BA.2.75.2, BQ.1.1 en XBB die waren 23 tot 63 keer zo laag als tegen WA1/2020.” |
| 71) Neutralisatie Ontsnapping door SARS-CoV-2 Omicron Subvarianten BA.2.12.1, BA.4 en BA.5, Hachmann, 2022 | “Zes maanden na de eerste twee BNT162b2-immunisaties was de mediane neutraliserende antilichaam-pseudovirustiter 124 tegen WA1/2020, maar minder dan 20 tegen alle geteste omicron-subvarianten. Twee weken na toediening van de boosterdosis nam de mediane neutraliserende antilichaamtiter aanzienlijk toe, tot 5783 tegen het WA1/2020-isolaat, 900 tegen de BA.1-subvariant, 829 tegen de BA.2-subvariant, 410 tegen de BA.2.12.1. subvariant, en 275 tegen de BA.4 of BA.5 subvariant. Onder de deelnemers met een voorgeschiedenis van Covid-19 was de mediane neutraliserende antilichaamtiter 11,050 tegen het WA1/2020-isolaat, 1740 tegen de BA.1-subvariant, 1910 tegen de BA.2-subvariant, 1150 tegen de BA.2.12.1-subvariant , en 590 tegen de BA.4 of BA.5 subvariant.” |
Uitgegeven onder a Creative Commons Naamsvermelding 4.0 Internationale licentie
Stel voor herdrukken de canonieke link terug naar het origineel Brownstone Instituut Artikel en auteur.









